Was du auf dieser Seite lernst
Du lernst, was eine Säure-Base-Titration ist, wie die Titrationskurve (pH vs. Volumen) aussieht und warum der Äquivalenzpunkt immer der Wendepunkt der Kurve ist. Außerdem berechnest du mit c(Säure) · V(Säure) = c(Base) · V(Base) die unbekannte Konzentration und lernst, wie man den richtigen Indikator auswählt.
Grundlagen – Kursstufe Säure-Base
Voraussetzungen für diese Seite: → Indikatoren und Umschlagbereich · → pH-Wert starker und schwacher Säuren · → Neutralisation (Kl. 9)
6. Säure-Base-Titration
Bei einer Titration handelt es sich um eine Neutralisationsreaktion unter kontrollierten Bedingungen: Man gibt schrittweise aus einer Bürette eine Maßlösung bekannter Konzentration zur Probelösung, bis der Äquivalenzpunkt erreicht ist – kenntlich am Farbumschlag des Indikators.
Die Titrationskurve zeigt den pH-Wert der Probelösung in Abhängigkeit vom Volumen der zugegebenen Maßlösung:
↑ Zum Vergrößern klicken
✕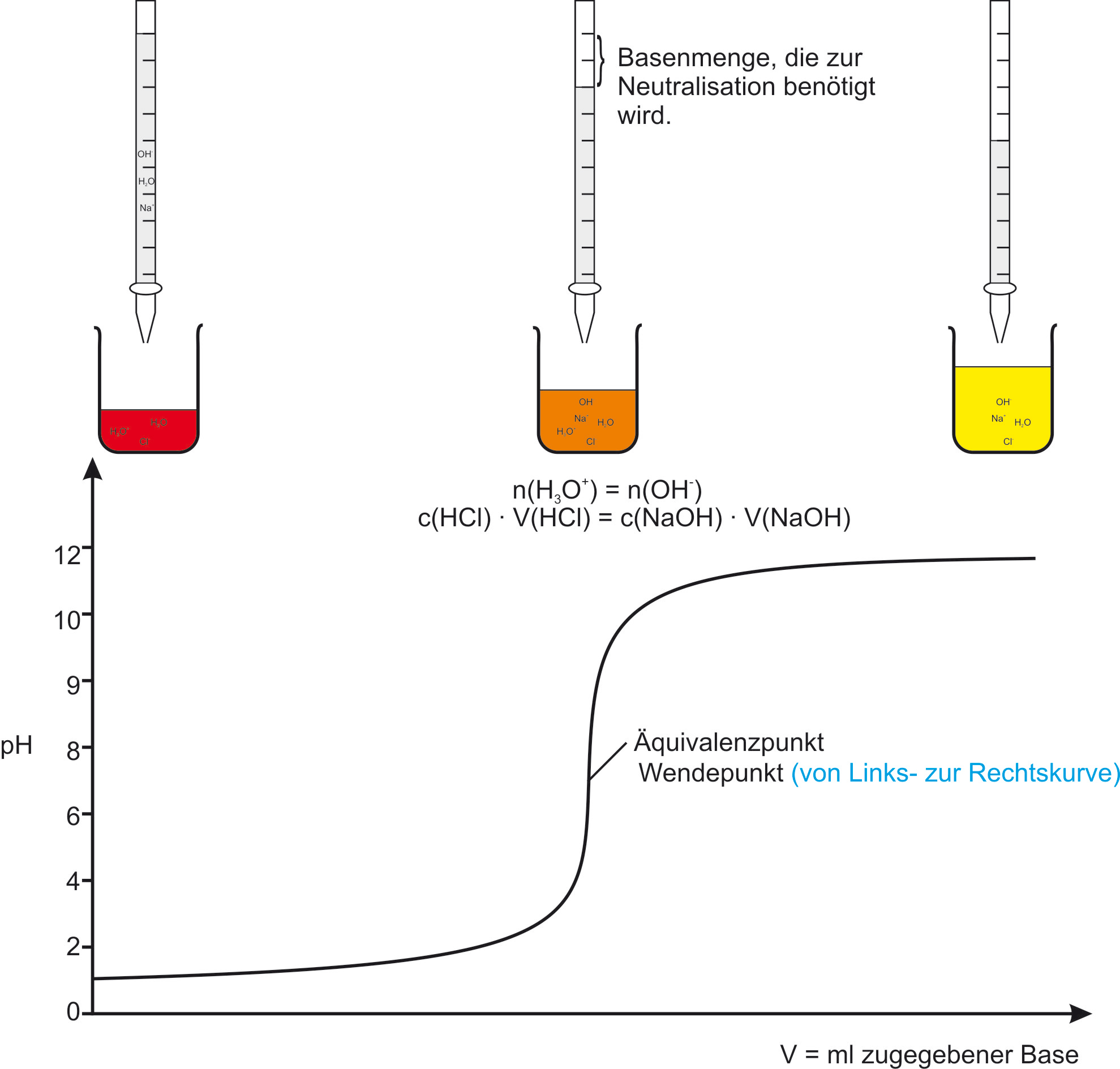
Die drei Phasen der Titration (Bsp. HCl + NaOH)
Vor dem ÄP
H3O+ + Cl− + H2O
pH niedrig · Indikator: Farbe 1
(z. B. rot)
Am Äquivalenzpunkt
Na+ + Cl− + H2O
n(H3O+) = n(OH−)
Indikator: Mischfarbe / Umschlag
Nach dem ÄP
Na+ + Cl− + H2O + OH−
pH hoch · Indikator: Farbe 2
(z. B. gelb)
Reaktionsgleichungen
Ausgangslösung: H3O+ + Cl− + H2O
Reaktion bis zum Äquivalenzpunkt:
H3O+ + Cl− + Na+ + OH− ⇌ 2 H2O + Na+ + Cl−
Lösung nach der Titration (jenseits des ÄP): Na+ + Cl− + H2O + OH−
Der Äquivalenzpunkt – Wendepunkt der Kurve
Am Äquivalenzpunkt (ÄP) haben genauso viele Protonen wie Hydroxidionen reagiert. Für die Titration von HCl mit NaOH gilt am ÄP:
n(H3O+) = n(OH−)
c(HCl) · V(HCl) = c(NaOH) · V(NaOH)
Der Äquivalenzpunkt ist gleichzeitig der Wendepunkt der Titrationskurve (Wechsel von der Links- zur Rechtskurve): Dort ist die Änderungsrate des pH-Werts am größten – ein kleiner Tropfen Maßlösung bewirkt einen sehr großen pH-Sprung.
Warum möglichst konzentrierte Maßlösung? Jede zugegebene Maßlösung verdünnt die Probelösung. Eine konzentrierte Maßlösung minimiert die Volumenzunahme und damit die Verdünnungs-Verfälschung des pH-Werts.
Berechnung: unbekannte Konzentration bestimmen
Kennt man das Volumen der Probelösung V(Säure), das Volumen der verbrauchten Maßlösung V(Base) am ÄP und die Konzentration der Maßlösung c(Base), so berechnet sich die gesuchte Konzentration der Probe:
c(Säure) = c(Base) · V(Base) / V(Säure)
Diese Beziehung gilt allgemein für einprotonige Säuren/Basen. Bei mehrprotonigen Säuren (z. B. H2SO4) muss die Wertigkeit berücksichtigt werden: n(Säure) · z(Säure) = n(Base) · z(Base).
Indikatorwahl: starke vs. schwache Säure
Die Wahl des Indikators hängt vom pH am Äquivalenzpunkt ab. Der pKS(HIn) des Indikators muss nahe am ÄP liegen (→ Indikatoren):
Starke Säure + starke Base
ÄP bei pH = 7
Großer pH-Sprung (ca. 4 → 10)
→ fast jeder Indikator geeignet
Empfehlung: Bromthymolblau, Lackmus
Schwache Säure + starke Base
ÄP bei pH > 7 (Salzhydrolyse)
Kleinerer pH-Sprung
Empfehlung: Phenolphthalein (pKS ≈ 9,4)
Starke Säure + schwache Base
ÄP bei pH < 7
Empfehlung: Methylorange (pKS ≈ 3,5) oder Methylrot
Auf einen Blick – die wichtigsten Aussagen
Äquivalenzpunkt
n(H3O+) = n(OH−)
= Wendepunkt der Titrationskurve
Berechnung
c · V = c · V
→ c(unbekannt) = c · V / V
Titrationskurve
Stark + stark: Sprung pH 4→10
Schwach + stark: Sprung kleiner,
ÄP > 7
Indikatorwahl
pKS(HIn) muss nahe dem
Äquivalenzpunkt liegen
Häufige Fragen – Säure-Base-Titration
Was ist der Äquivalenzpunkt und warum ist er der Wendepunkt der Kurve?
Am Äquivalenzpunkt haben genauso viele H3O+-Ionen wie OH−-Ionen reagiert: n(H3O+) = n(OH−). Mathematisch ist er der Wendepunkt der pH-Kurve (Wechsel von Links- zu Rechtskrümmung), weil dort die pH-Änderung pro zugegebenem Volumen am größten ist – ein minimaler Überschuss an Maßlösung erzeugt einen großen pH-Sprung. Den ÄP erkennt man im Experiment am Farbumschlag des Indikators.
Wie berechnet man die Konzentration einer unbekannten Säure bei der Titration?
Aus der Bedingung am Äquivalenzpunkt (n(Säure) = n(Base)) folgt: c(Säure) · V(Säure) = c(Base) · V(Base). Umgestellt: c(Säure) = c(Base) · V(Base) / V(Säure). Beispiel: 20 mL unbekannte HCl-Lösung werden mit 25 mL NaOH (c = 0,1 mol/L) titriert: c(HCl) = 0,1 · 25 / 20 = 0,125 mol/L.
Warum liegt der Äquivalenzpunkt bei einer schwachen Säure + starker Base nicht bei pH 7?
Am ÄP entsteht das Salz der schwachen Säure. Das Anion (z. B. Acetat−) hydrolysiert als schwache Base mit Wasser und bildet OH−-Ionen → die Lösung ist schwach basisch. Je schwächer die titrierte Säure (je größer pKS), desto höher der pH am ÄP. Ausführlich: Säure-Base-Reaktionen in Salzlösungen.
Warum sollte die Maßlösung möglichst konzentriert sein?
Jeder Tropfen Maßlösung, der zugegeben wird, verdünnt die Probelösung. Bei einer konzentrierten Maßlösung braucht man weniger Volumen für dieselbe Stoffmenge, die Volumenzunahme – und damit die Verfälschung des pH-Werts durch Verdünnung – bleibt gering. Das macht die Titrationskurve schärfer und den Äquivalenzpunkt leichter erkennbar.
Welchen Indikator verwendet man für eine Titration mit Phenolphthalein?
Phenolphthalein (pKS ≈ 9,4, Umschlag pH 8,2–10) eignet sich für Titrationen, bei denen der Äquivalenzpunkt im schwach basischen Bereich liegt, also für die Titration einer schwachen Säure mit einer starken Base (z. B. Essigsäure + NaOH, ÄP ≈ pH 8,9). Für starke Säure + starke Base (ÄP = pH 7) sind Bromthymolblau oder Lackmus besser geeignet. Mehr: Indikatoren.
Lernkarten – Säure-Base-Titration
Klicke auf eine Karte, um die Antwort zu sehen.
Was gilt am Äquivalenzpunkt einer Titration?
n(H3O+) = n(OH−)
→ c(Säure) · V(Säure) = c(Base) · V(Base)
Der ÄP ist der Wendepunkt der Titrationskurve.
Wie bestimmt man c(Säure) aus einer Titration?
c(Säure) = c(Base) · V(Base) / V(Säure)
V(Base) = Volumen der Maßlösung am ÄP (abgelesen an der Bürette)
Warum liegt der ÄP bei Schwache-Säure + Starke-Base nicht bei pH 7?
Das entstehende Salz-Anion hydrolysiert als schwache Base → OH− entsteht → Lösung ist schwach basisch (pH > 7).
Welcher Indikator eignet sich für HCl + NaOH?
ÄP bei pH = 7 → großer pH-Sprung (4→10).
Geeignet: Bromthymolblau (Umschlag 6–7,6)
oder Lackmus (5–8).
Phenolphthalein wäre zu spät (Umschlag 8,2–10).
Rechenaufgabe: 25 mL HCl werden mit 30 mL NaOH (c = 0,2 mol/L) titriert. Wie groß ist c(HCl)?
c(HCl) = c(NaOH) · V(NaOH) / V(HCl)
= 0,2 · 30 / 25
= 0,24 mol/L
Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← Indikatoren → Pufferlösungen
🔁 Grundlagen: Säure-Base-Reaktionen in Salzlösungen · Neutralisation (Kl. 9)
📌 Weiterführend: Pufferlösungen · Zusammenfassung Säure-Base 4.6
