9 Bildung von Calciumhydroxid aus Calciumoxid und Wasser
a) Bildung von Calciumhydroxid („Löschen von gebranntem Kalk“)
Hierfür wird in einem Experiment etwas Calcium(II)-Oxid in ein Reagenzglas gegeben und wenige Wasser zugetropft.
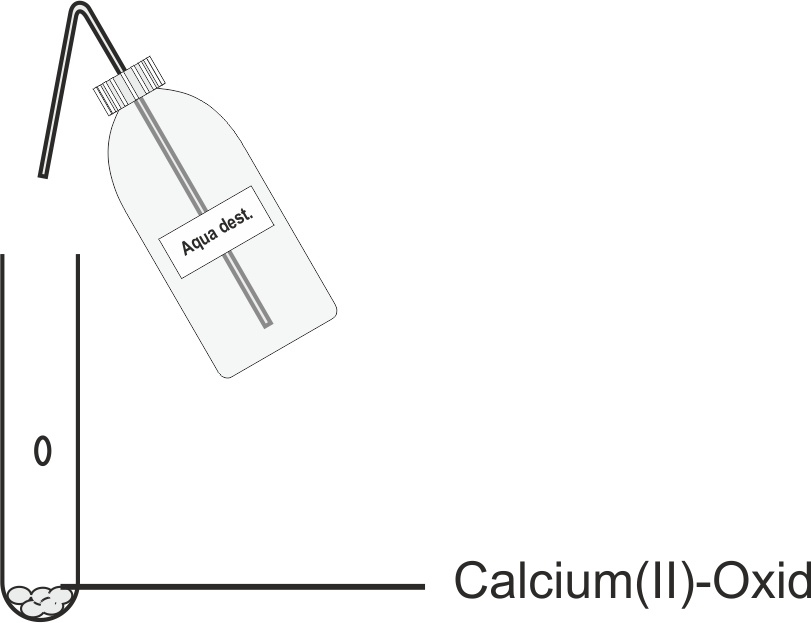
Beobachtung: Das Reagenzglas wird sehr heiß! Es ist also eine freiwillige, exotherme Reaktion.
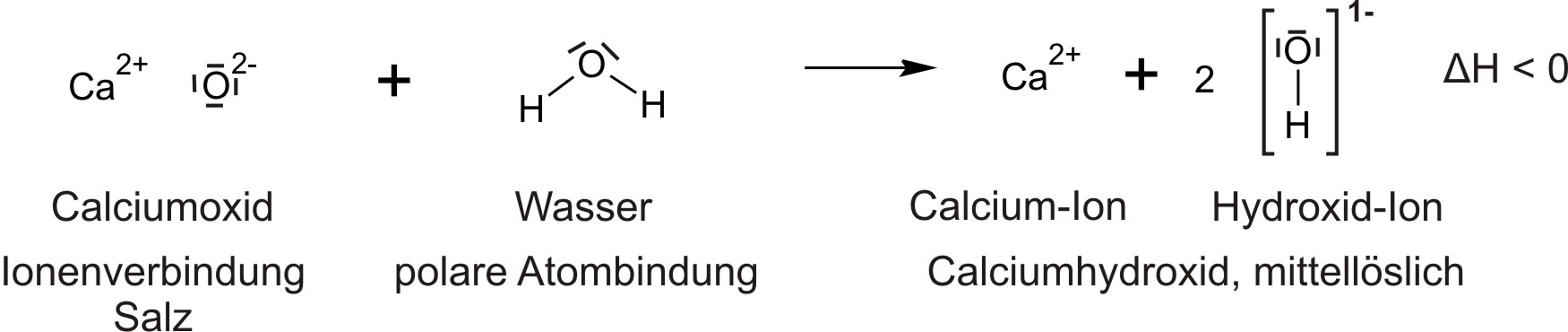
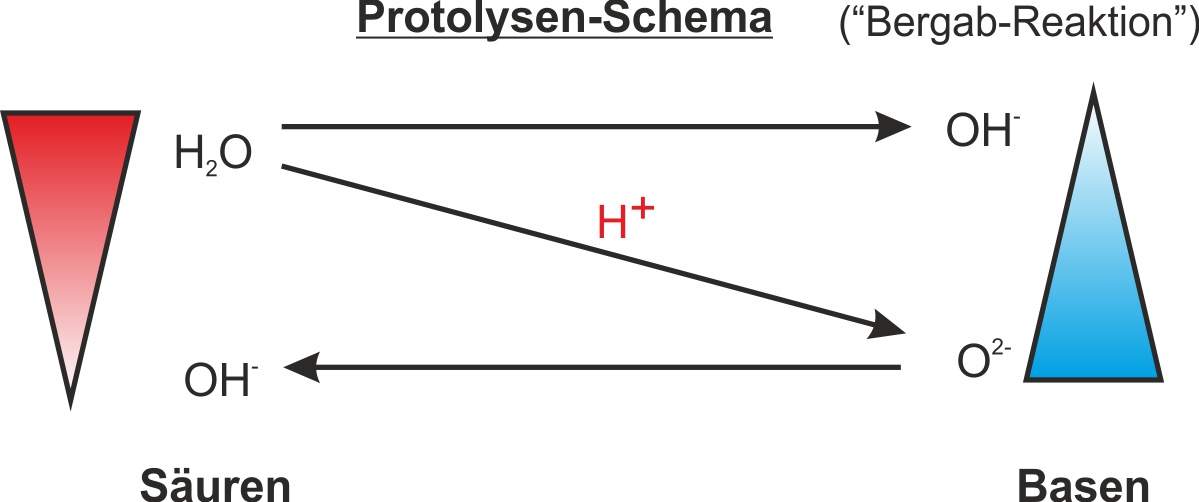
Aufgabe: Formuliert die Reaktionsgleichung mit Hilfe von Strukturformeln (formuliert hierfür auch die Teilchen als Ionen). Zeichnet dann auch noch eine Protolyse-Schema für dies Reaktion mit den Teilchen, die bei dieser Reaktion beteiligt sind.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
b) Erhitzen von Calciumhydroxid
Die oben genannte Reaktion kann man aber auch Umkehren. Da die Bildung von Calciumhydroxid freiwillige und exotherm verläuft muss die Umkehrung natürlich unter Zwang und endotherm (also Energie in Wärme muss in das System hingesteckt werden) verlaufen.
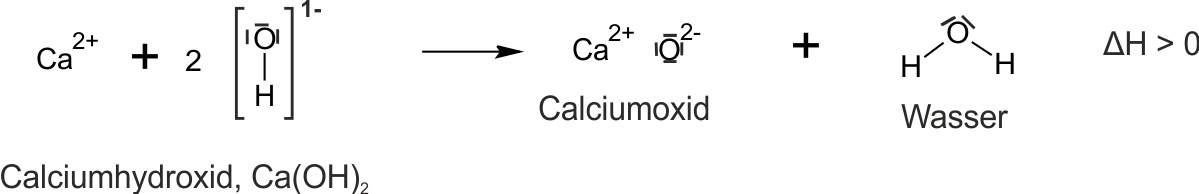
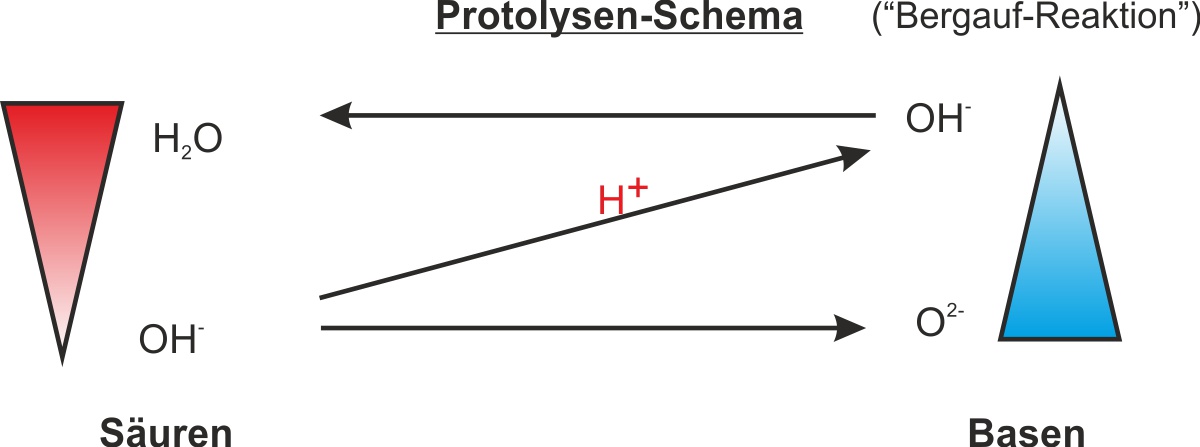
Aufgabe: Formuliert für die Umkehrung dieser Reaktion auch eine Reaktionsgleichung mit Hilfe von Strukturformeln und ein Protolyse-Schema. Wichtig für das Schema ist, dass die Säuren immer links stehen, die starke Säure oben links und die starke Base unten rechts. Außerdem zeigt der diagonale Pfeil an, ob eine Reaktion freiwillig ("bergab" = von oben nach unten) oder unfreiwillig ("bergauf" = von unten nach oben) verläuft.
{slider title="Lösung" open="false" class="icon"}
{/sliders}