Ammoniak
-
2 Reaktion von Chlorwasserstoff-Gas mit Ammoniak-Gas
2 Reaktion von Chlorwasserstoff-Gas mit Ammoniak-Gas
Hinweis: Um die Vorgänge besser nachvollziehen zu können gibt es hier ein Periodensystem der Elemente-Popup
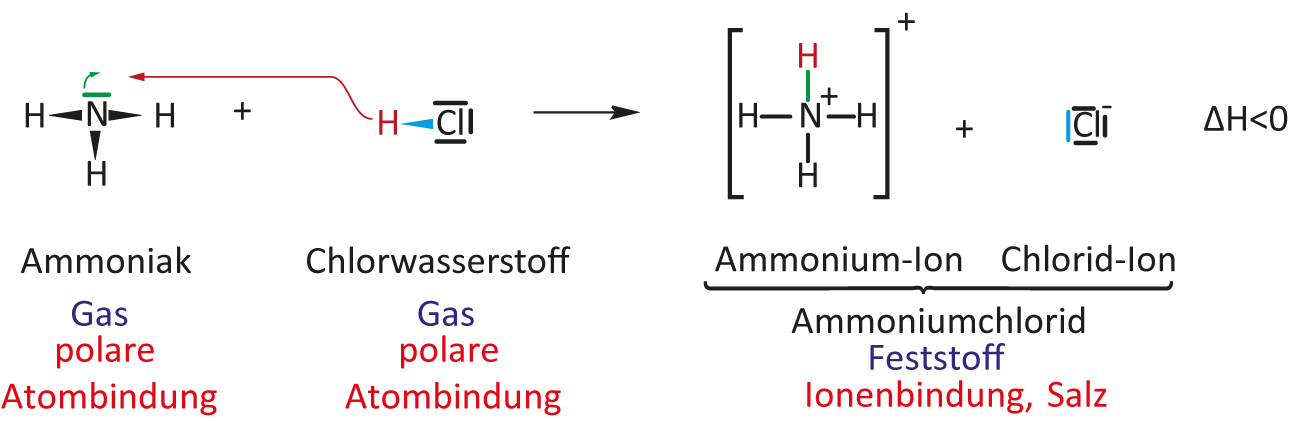
Bei diesen zwei Teilchen liegen polare Atombindungen vor:
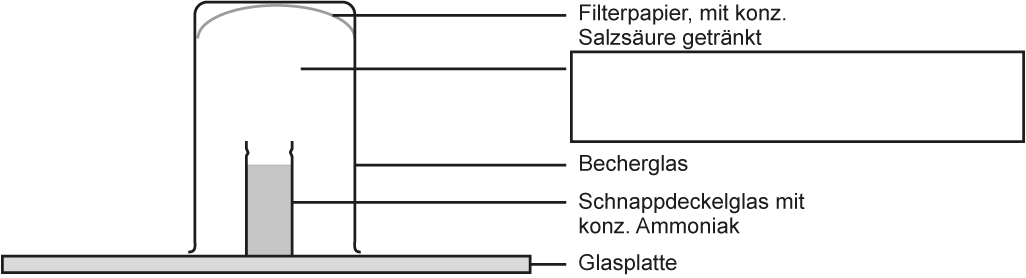
a) Versuch mit Skizze: (vgl. AB )
b) Beobachtung:
Innerhalb des Becherglas bildet sich weißer Rauch. Am Boden der Glasplatte setzt sich ein weißer, kristalliner Stoff ab.
Vorher:
Nachher:
c) Auswertung:
I. Teilchengleichung:NH₃ + HCl → NH₄¹⁺Cl¹⁻
II. Reaktionsgleichung (Stoffgleichung)
NH₃ (g) + HCl (g) → NH₄Cl (s) ΔH < 0III. Protolyse-Schema
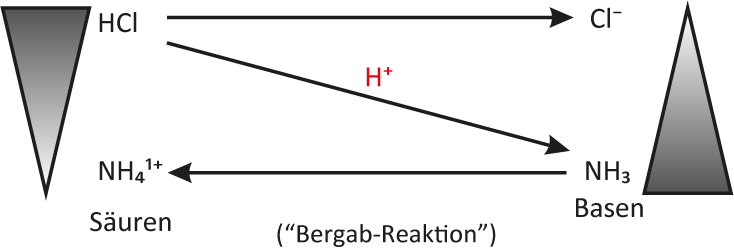
Aufgabe: Skizziert einmal das Protolyse-Schema für diese chemische Reaktion. Tipp: Falls Ihr noch Schwierigkeiten damit habt, schaut nochmal das allgemeine Beispiel an.
{slider title="Lösung: Protolyse-Schema für die Bildung von Ammoniumchlorid" open="false" class="icon"}
{/sliders}
-
3 Reaktion von festem Ammoniumchlorid und festem Natriumhydroxid
3 Reaktion von festem Ammoniumchlorid und festem Natriumhydroxid
a) Versuch mit Skizze
Die beiden Salze NH₄Cl und NaOH werden gemeinsam im Mörser zerrieben. Nach dem Zerreiben wird ein angefeuchtetes Indikatorpapier über die Schale gehalten; zusätzlich wird eine Geruchsprobe vorgenommen.
b) Beobachtung:Es entsteht ein stechend riechendes Gas. Das feuchte Indikatorpapier färbt sich blau. Die Festsubstanz im Mörser wird feucht.
c) Auswertung:
I. Teilchengleichung
II. ReaktionsgleichungNH₄Cl + NaOH → NH₃ + NaCl + H₂O Ammoniumchlorid Natriumhydroxid Ammoniak Natriumchlorid Wasser III. Protolysenschema
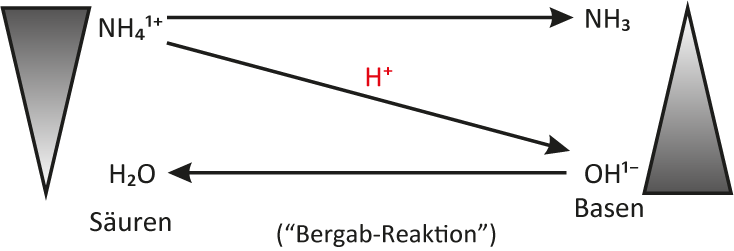
Aufgabe: Formuliert für diese chemische Reaktion ein Protolyse-Schema
{slider title="Lösung: Protolyse-Schema für das Verreiben von Ammoniumchlorid und Natriumhydroxid" open="false" class="icon"}
{/sliders}
-
4.4 Der räumliche Bau von Molekülen
4.4 Der räumliche Bau von Molekülen
{slider title="Link zur interaktiven Übungsseiten mit Bildern" open="false" class="icon"}
Etwas genauer, mit mehr Abbildungen gibt es auf der Basischemie-Seite. Zum Lernen vielleicht besser geeignet. Den Tafelanschrieb gibt es aber komprimierter auf dieser Seite.
Übungsseiten zum räumlichen Bau von Molekülen
{/sliders}
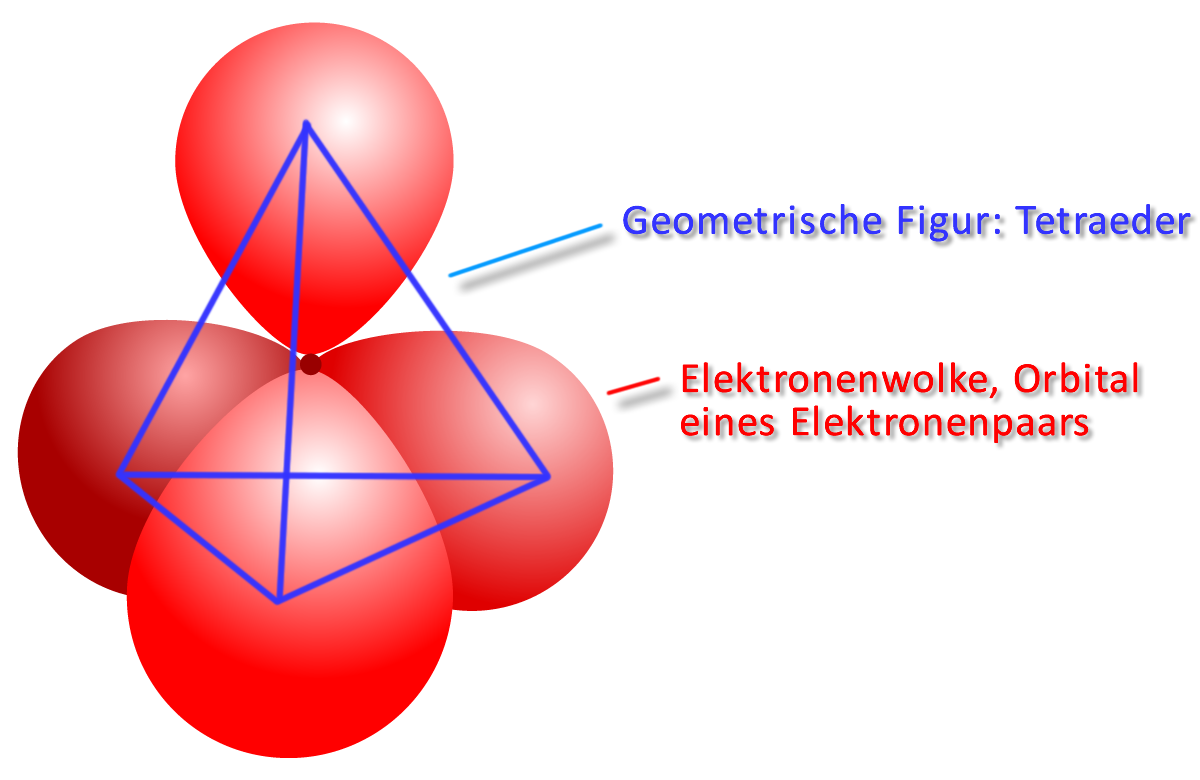
Im Kugelwolkenmodell ordnen sich die vier energetisch gleichwertigen Orbitale tetraedrisch an. Durch die gegenseitige Abstoßung (durch die gleiche, negative Ladung der Elektronen) der „Elektronenwolke“ erreichen sie so den größtmöglichen Abstand voneinander: Tetraederwinkel: 109,5 °
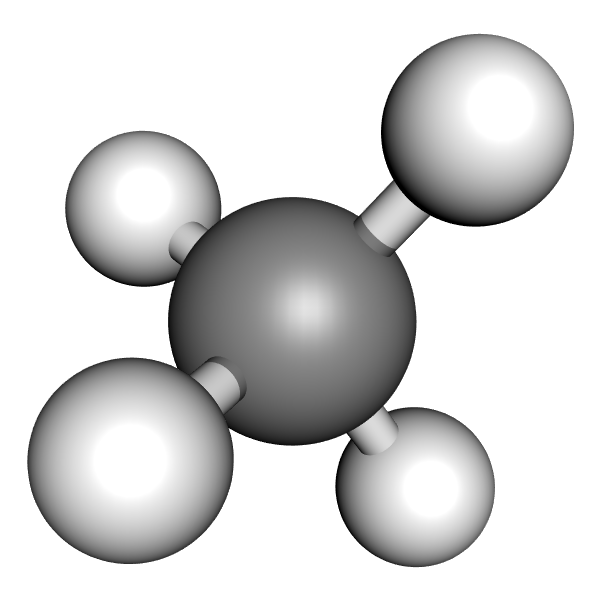
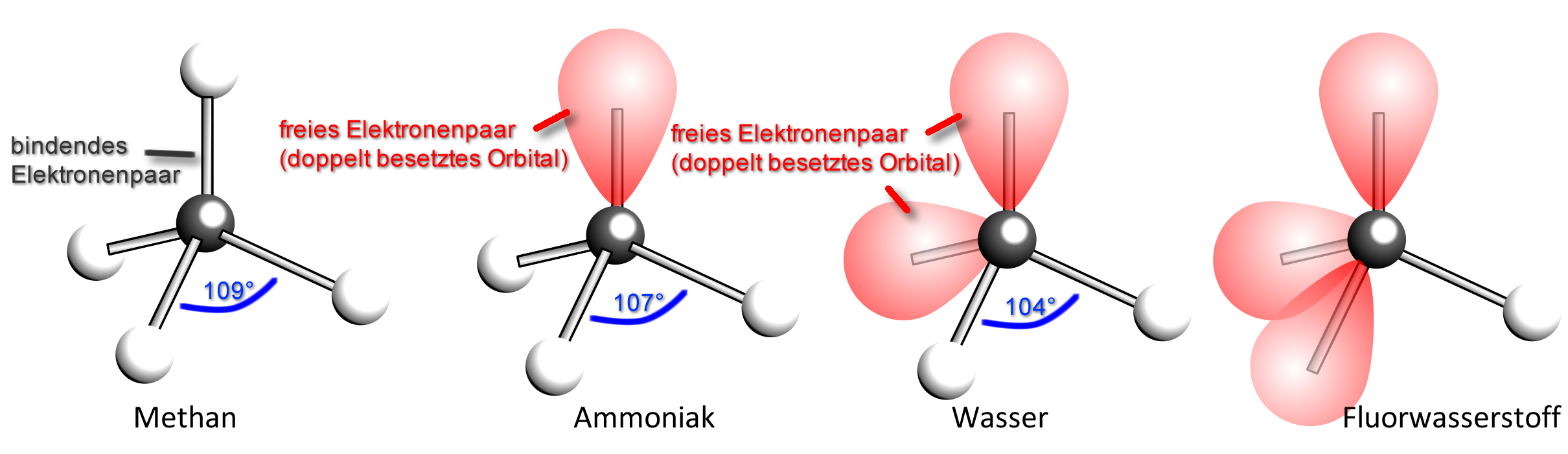
a) Das Methan-Molekül (CH₄)
Die 4 Wasserstoff-Atome sind tetraedrisch um das Kohlenstoff-Atom angeordnet. Die bindenden Elektronenpaare haben somit den größtmöglichen Abstand voneinander.
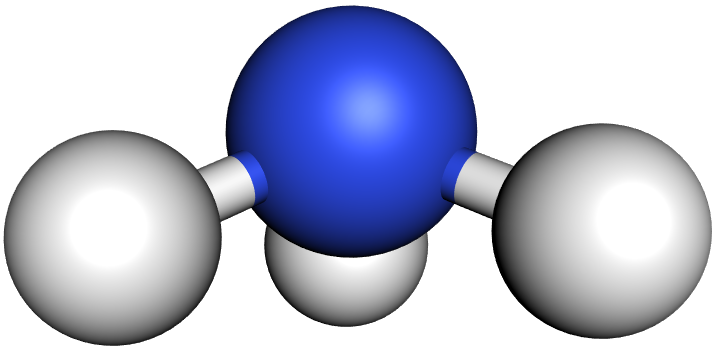
b) Das Ammoniak-Molekül (NH₃):
Im Ammoniak-Molekül stoßen sich die drei bindenden und das eine freie Elektronenpaar gegenseitig ab. Die Winkel zwischen den bindenden Elektronenpaaren sind jedoch nur 107° (statt 109,5°).
Erklärung(durch Zusatzannahmen): Die „Elektronenwolke“ eines nichtbindenden Elektronenpaares nimmt einen größeren Raumbereich ein als die eines Bindungselektronenpaars. Sie drückt daher die anderen „Elektronenwolken“ etwas näher zusammen. Der Bindungswinkel wird kleiner.
Merke: Nichtbindende Elektronenpaare nehmen einen größeren Raum ein als bindende Elektronenpaare. Info für Interessierte: Das oben genanntes Modell ist ein vereinfachtes VSEPR-Modell (Abkürzung für englisch valence shell electron pair repulsion, deutsch Valenzschalen-Elektronenpaar-Abstoßung), auch EPA-Modell (Elektronenpaarabstoßungs-Modell)
-
5 Stärke von Säuren und Basen
5 Stärke von Säuren und Basen - Säurestärke und Molekülstruktur
Hinweis 1: Das Kapitel stammt aus dem Oberstufenbereich. Ich halte es für das Verständnis für Säure-Base-Reaktionen wichtig, weil man sonst bei einer Reaktion mit zwei Ampholyten (z.B. Wasser und Ammoniak) gar nicht weiß, wer die Säure ist und wer als Base funktioniert.
Hinweis 2: Auch hier ist es von Vorteil, wenn man ein Periodensystem der Elemente zur Hand hat.
Brønsted-Theorie:
Säurestärke ist die Tendenz Protonen abzugeben.
Basenstärke Tendenz Protonen aufzunehmen.Bsp. HCl + H₂O → H₃O⁺ + Cl⁻
Säure 1 Base 2 Säure 2 Base 1Info: Supersäuren = Säuren die stärker als H₂SO₄ sind.
Je stärker die Säure desto schwächer die konjugierte (korrespondierende) Base.
5.1 Binäre Säuren.
Faktoren für Säurestärke von Bedeutung:
- Elektronegativität (innerhalb einer Periode)
- Atomgröße (innerhalb einer Gruppe)
a) innerhalb einer Periode (binäre H-Verbindungen)
Säurestärke nimmt mit der EN zu (Atomgrößenunterschiede sind „zu“ gering)
⇨ Elektronen werden stärker dem H-Atom entzogen ⇨ erleichterte Protonenabspaltung.Bsp.:
2. Periode:
Zunahme der EN: N < O < F
Zunahme der Säurestärke NH₃ < H₂O < HF
Gegenüber Wasser Base Säure
3. Periode
Zunahme der EN: P < S < Cl
Zunahme der Säurestärke PH₃ < H₂S < HCl
b) innerhalb einer Gruppe (binäre H-Verbindungen):
Säurestärke nimmt mit der Atomgröße zu (stärkere Auswirkung als Elektronegativität)
⇨ bei einem großen Atom ist die Valenzelektronenwolke auf einem größeren Raum verteilt ⇨ H⁺ ist weniger fest gebunden.H₂O < H₂S < H₂Se < H₂Te
HF < HCl < HBr < HI5.2 Oxosäuren

Sauerstoff hat in etwa die gleiche Größe
a) EN von Z ist entscheidend.
Je größer die EN von Z, desto stärker ist die Säure (-I-Effekt).HOI < HOBr < HOCl
hyopoiodige Säure hypobromige hypochlorige Säureb) An Z sind weitere O-Atome gebunden ⇨ stärkerer –I-Effekt (bzw. höhere Formalladung am Z. )
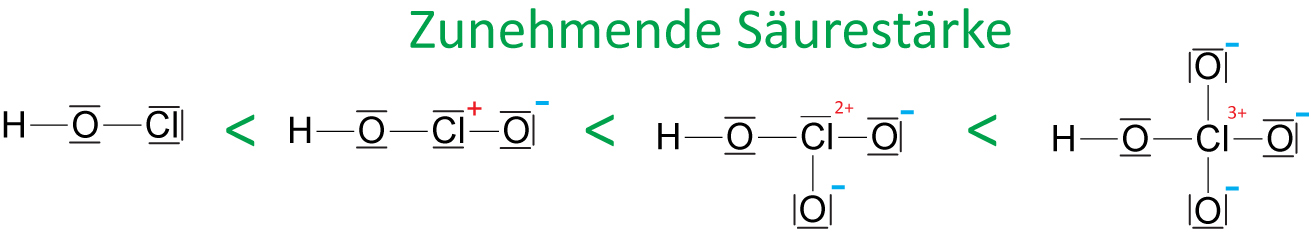
hypochlorige – chlorige – Chlor – Perchlorsäuren
⇨ Man kann Säurestärke abschätzen: Je mehr mehr O-Atome an das Z-Atom jedoch nicht an H-Atom gebunden sind, desto die Säure:
H-O-NO < H-O-NO₂
salpetrige Säure Salpetersäure
(H-O-)₂SO < (H-O-)₂SO₂
schweflige Säure Schwefelsäure