Was du auf dieser Seite lernst
Hier lernst du, wie die Basenstärke mit dem pKB-Wert quantitativ beschrieben wird und wie die Basenkonstante KB berechnet wird. Außerdem zeigt dir Abschnitt 4.3 die wichtige Beziehung pKS + pKB = pKW = 14 zwischen einem korrespondierenden Säure-Base-Paar.
Grundlagen aus der 9. Klasse
Die Grundlagen zu Säuren, Basen und korrespondierenden Paaren hast du bereits in der 9. Klasse kennengelernt: → Säure-Base-Definition nach Brønsted (Kl. 9)
4.2 Basestärke: der pKB-Wert
Als Maß für die Stärke einer Base dient das Ausmaß ihrer Reaktion mit Wasser:
Allgemeines Beispiel:
A1− + H2O ⇌ HA + OH−
↑ Zum Vergrößern klicken
✕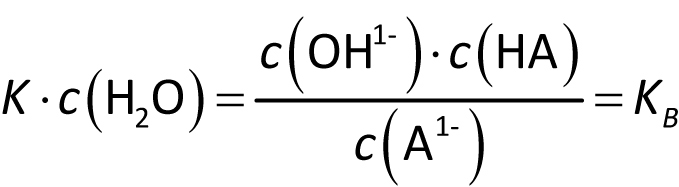
KB ist die Basenkonstante. Auch hier gibt man meist den negativen dekadischen Logarithmus an:
pKB = − log KB
↑ Zum Vergrößern klicken
✕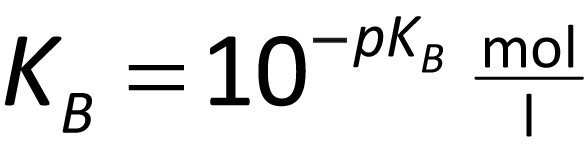
4.3 Beziehung zwischen KS und KB eines korrespondierenden Säure-Base-Paares
HA ist eine beliebige Säure und A1− ihre konjugierte (korrespondierende) Base.
HA + H2O ⇌ A1− + H3O+ H2O + A1− ⇌ OH− + HA
↑ Zum Vergrößern klicken
✕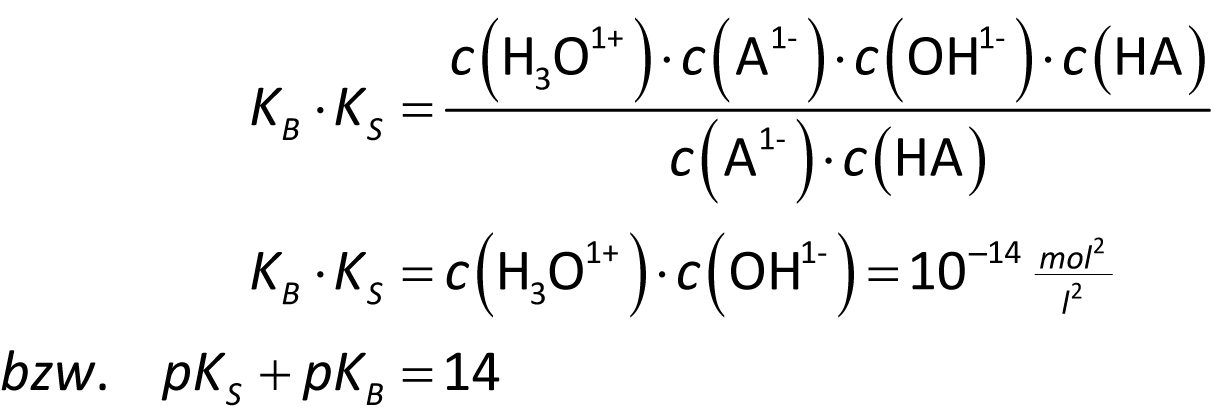
Merke: Ist der pKS-Wert einer Säure bekannt (Tabelle), so kann man mit obiger Gleichung den pKB-Wert berechnen (und umgekehrt).
Die obige Gleichung zeigt auch: Je stärker eine Säure ist, desto schwächer ist ihre korrespondierende Base (und umgekehrt).
Bsp.:
Oxonium-Ion: KS = 55 pKS = −1,74 (sehr starke Säure)
Wasser (korrespondierende Base): pKB = 15,74 (sehr schwache Base)
Auf einen Blick – die wichtigsten Aussagen
pKB-Wert
Je kleiner der pKB-Wert, desto stärker ist die Base. pKB = −log KB
Basenkonstante KB
KB ist die Gleichgewichtskonstante der Protolyse einer Base mit Wasser: A⁻ + H₂O ⇌ HA + OH⁻
pKS + pKB = 14
Bei 25 °C gilt für jedes korrespondierende Säure-Base-Paar: pKS + pKB = pKW = 14
Konjugiertes Paar
Je stärker eine Säure, desto schwächer ihre korrespondierende Base – und umgekehrt.
Häufige Fragen – pKB-Wert und Basenstärke
Was ist der pKB-Wert und wofür wird er verwendet?
Der pKB-Wert ist der negative dekadische Logarithmus der Basenkonstante KB: pKB = −log KB. Er gibt an, wie stark eine Base mit Wasser reagiert (Protolysegrad). Je kleiner der pKB-Wert, desto stärker ist die Base. Starke Basen (z. B. OH⁻) haben sehr kleine oder negative pKB-Werte, schwache Basen (z. B. Ammoniak mit pKB ≈ 4,7) haben größere Werte.
Wie ist die Basenkonstante KB definiert?
KB ist die Gleichgewichtskonstante der Reaktion einer Base A⁻ mit Wasser: A⁻ + H₂O ⇌ HA + OH⁻. Sie berechnet sich aus dem Verhältnis der Gleichgewichtskonzentrationen der Produkte zu der des Edukts (Wasser wird nicht berücksichtigt, da es als Lösungsmittel im großen Überschuss vorliegt). Auf der Seite Säurestärke – der pKS-Wert findest du die analoge Definition für Säuren.
Wie hängen pKS- und pKB-Wert eines korrespondierenden Paares zusammen?
Bei 25 °C gilt: pKS + pKB = pKW = 14. Diese Beziehung folgt daraus, dass KS · KB = KW = 10⁻¹⁴. Kennt man den pKS-Wert einer Säure aus einer Tabelle, so erhält man den pKB-Wert der konjugierten Base einfach durch: pKB = 14 − pKS. Mehr zur Autoprotolyse des Wassers und pKW.
Warum ist Wasser eine extrem schwache Base?
Das Oxonium-Ion H3O+ ist eine sehr starke Säure (pKS = −1,74). Nach der Beziehung pKS + pKB = 14 ergibt sich für die korrespondierende Base Wasser: pKB(H2O) = 14 − (−1,74) = 15,74. Wasser reagiert also kaum als Base mit Wasser – es hat praktisch keine Neigung, ein Proton von einem anderen Wassermolekül aufzunehmen.
Welche praktische Aussage lässt sich aus der pKS/pKB-Beziehung ableiten?
Die Beziehung zeigt, dass korrespondierende Paare immer „Gegenspieler" sind: Eine starke Säure hat eine schwache konjugierte Base, und umgekehrt. Das ist wichtig für die Berechnung des pH-Werts von Salzlösungen oder für das Verständnis von Pufferlösungen, bei denen eine schwache Säure und ihre korrespondierende Base zusammenwirken.
Lernkarten – pKB-Wert und Basenstärke
Klicke auf eine Karte, um die Antwort zu sehen.
Was bedeutet der pKB-Wert und was sagt er über eine Base aus?
pKB = −log KB ist der negative Logarithmus der Basenkonstante. Je kleiner pKB, desto stärker ist die Base.
Wie lautet die allgemeine Gleichung für die Protolyse einer Base A⁻ mit Wasser?
A⁻ + H₂O ⇌ HA + OH⁻
Die Basenkonstante KB beschreibt das Gleichgewicht dieser Reaktion.
Welche zentrale Beziehung gilt für ein korrespondierendes Säure-Base-Paar bei 25 °C?
pKS + pKB = pKW = 14
(folgt aus KS · KB = KW = 10⁻¹⁴)
Was folgt für die korrespondierende Base, wenn ihre Säure sehr stark ist?
Je stärker die Säure (kleiner pKS), desto schwächer die korrespondierende Base (größer pKB) – und umgekehrt.
Rechenaufgabe: Der pKS-Wert der Essigsäure beträgt 4,75. Wie groß ist der pKB-Wert des Acetat-Ions?
pKB(Acetat⁻) = 14 − 4,75 = 9,25
Das Acetat-Ion ist eine sehr schwache Base (reagiert kaum mit Wasser).
Weiter im Kapitel Säure-Base-Reaktionen (Kursstufe)
← Säurestärke – der pKS-Wert → pH-Wert verschieden starker Säuren
🔁 Grundlagen: Säure-Base-Definition nach Brønsted (Kl. 9) · Autoprotolyse des Wassers – pKW
📌 Weiterführend: Pufferlösungen · Säure-Base-Reaktionen in Salzlösungen
