2 Fischer-Projektion
Regeln und Reihenfolge:
- C-Gerüst senkrecht
- höchstes oxidiertes C-Atom oben (Oxidationszahl)
- beide C-C-Bindungen am mittleren C-Atom zeigen nach hinten (hinter die Papier-Ebene)
- beide horizontale Bindungen am mittleren, asymmetrischen C-Atom (H-C-; H-O-C-Bindung) zeigen nach vorne.
- Das Isomer, bei dem die Substituentengruppe mit dem elektronegativsten Atom in der Fischer-Projektion rechts steht, wird mit D[1] bezeichnet; steht der Substituent links, dann wird er mit L[2] bezeichnet.
Beispiel
a) Milchsäure: 2 Hydroxypropansäure
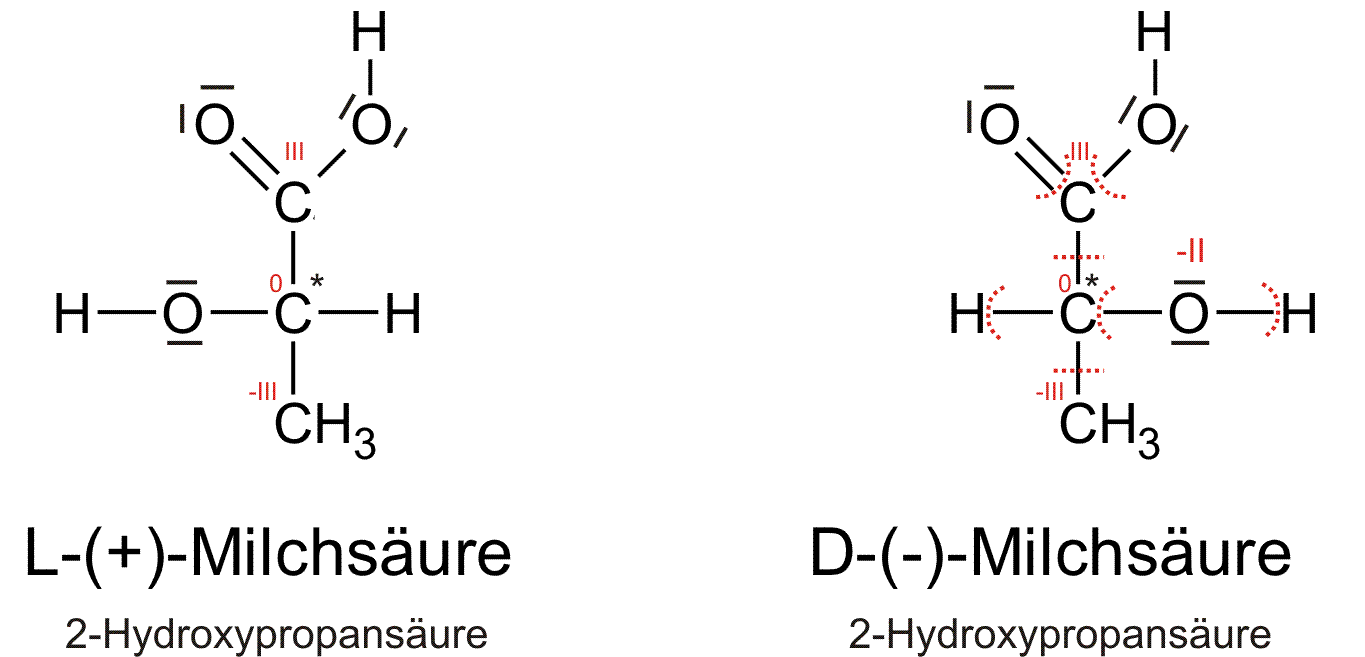
Im folgenden die D-Milchsäure
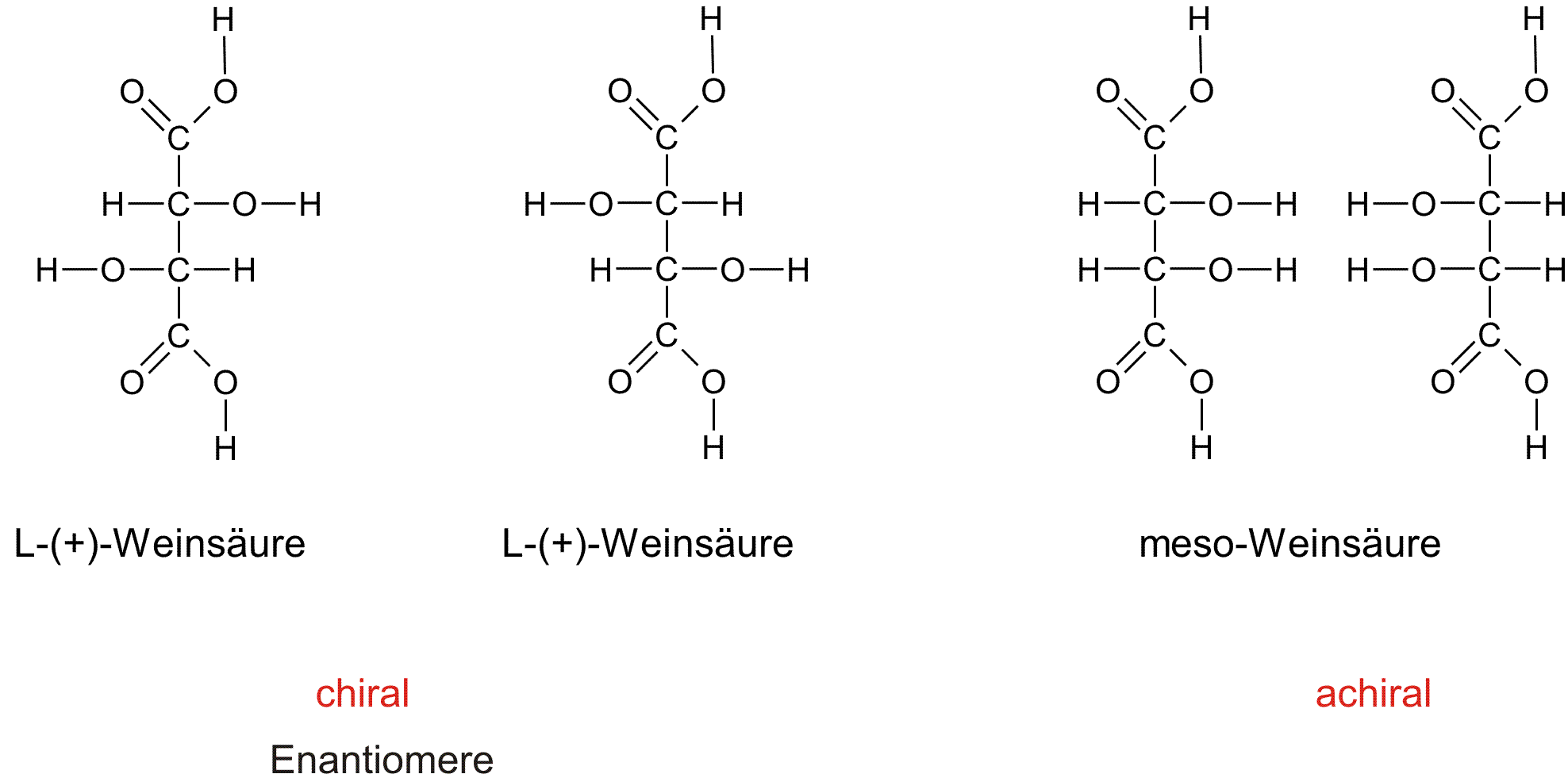
c) Weinsäure (2,3-Dihydroxybutan-1,4-Dicarbonsäure):
Wichtiger Hinweis: die zweite Weinsäure ist die D-(-)-Weinsäure. Der Name innerhalb der Abbildung ist falsch! Danke für die Korrektkur.
Hat eine Verbindung n asymmetrische C-Atome, so gibt es meist 2n Stereoisomere. Stereoisomere, die keine Enantiomere sind, heißen Diastereomere und haben verschiedene physikalische Eigenschaften.
Substanzen, deren Moleküle mit ihren Spiegelbildern übereinstimmen, obwohl sie Chiralitätszentranen besitzen, heißen meso-Verbindungen ("Das Spiegelbild des Originals kann durch Drehung wieder genau so aussehen, wie das Original). Sie besitzen eine Spiegelebene im Molekül.
-----------------
[1] D = dexter (lat) = rechts
[2] L = laevus (lat) = links
