Alkanone
-
02 Fischer-Projektion
2 Fischer-Projektion
Regeln und Reihenfolge:
- C-Gerüst senkrecht
- höchstes oxidiertes C-Atom oben (Oxidationszahl)
- beide C-C-Bindungen am mittleren C-Atom zeigen nach hinten (hinter die Papier-Ebene)
- beide horizontale Bindungen am mittleren, asymmetrischen C-Atom (H-C-; H-O-C-Bindung) zeigen nach vorne.
- Das Isomer, bei dem die Substituentengruppe mit dem elektronegativsten Atom in der Fischer-Projektion rechts steht, wird mit D[1] bezeichnet; steht der Substituent links, dann wird er mit L[2] bezeichnet.
Beispiel
a) Milchsäure: 2 Hydroxypropansäure
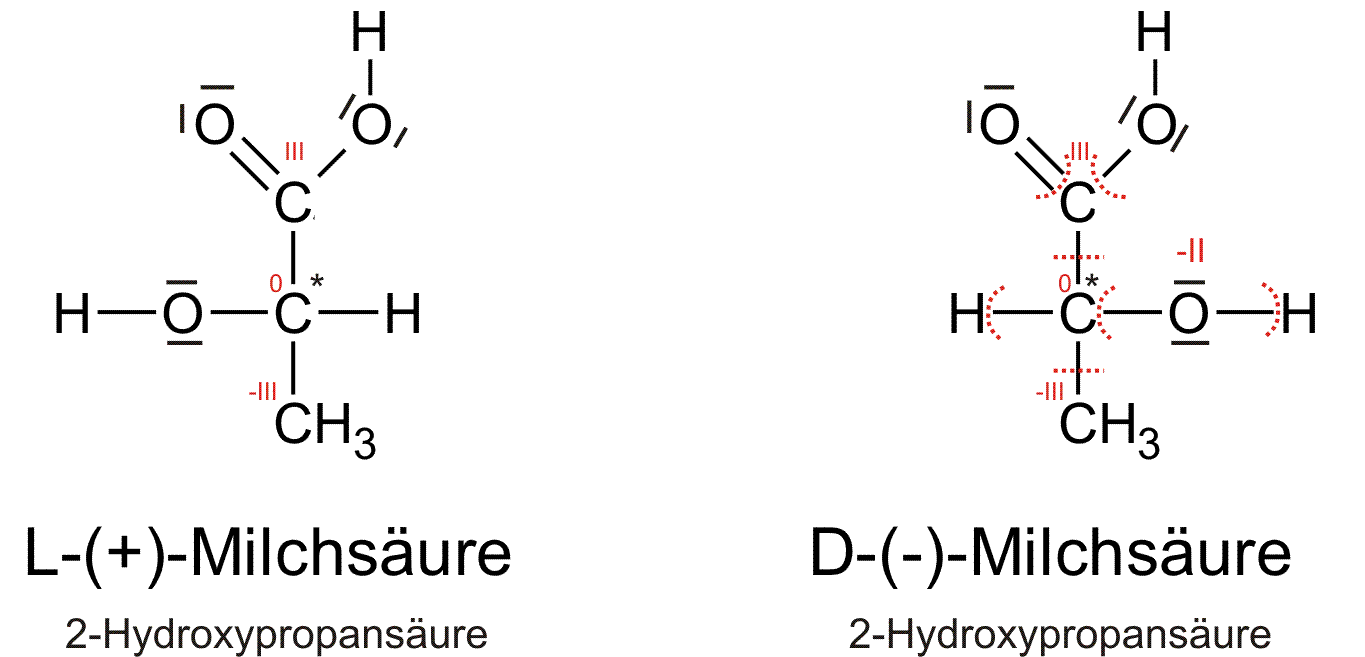
Im folgenden die D-Milchsäure
c) Weinsäure (2,3-Dihydroxybutan-1,4-Dicarbonsäure):
Wichtiger Hinweis: die zweite Weinsäure ist die D-(-)-Weinsäure. Der Name innerhalb der Abbildung ist falsch! Danke für die Korrektkur.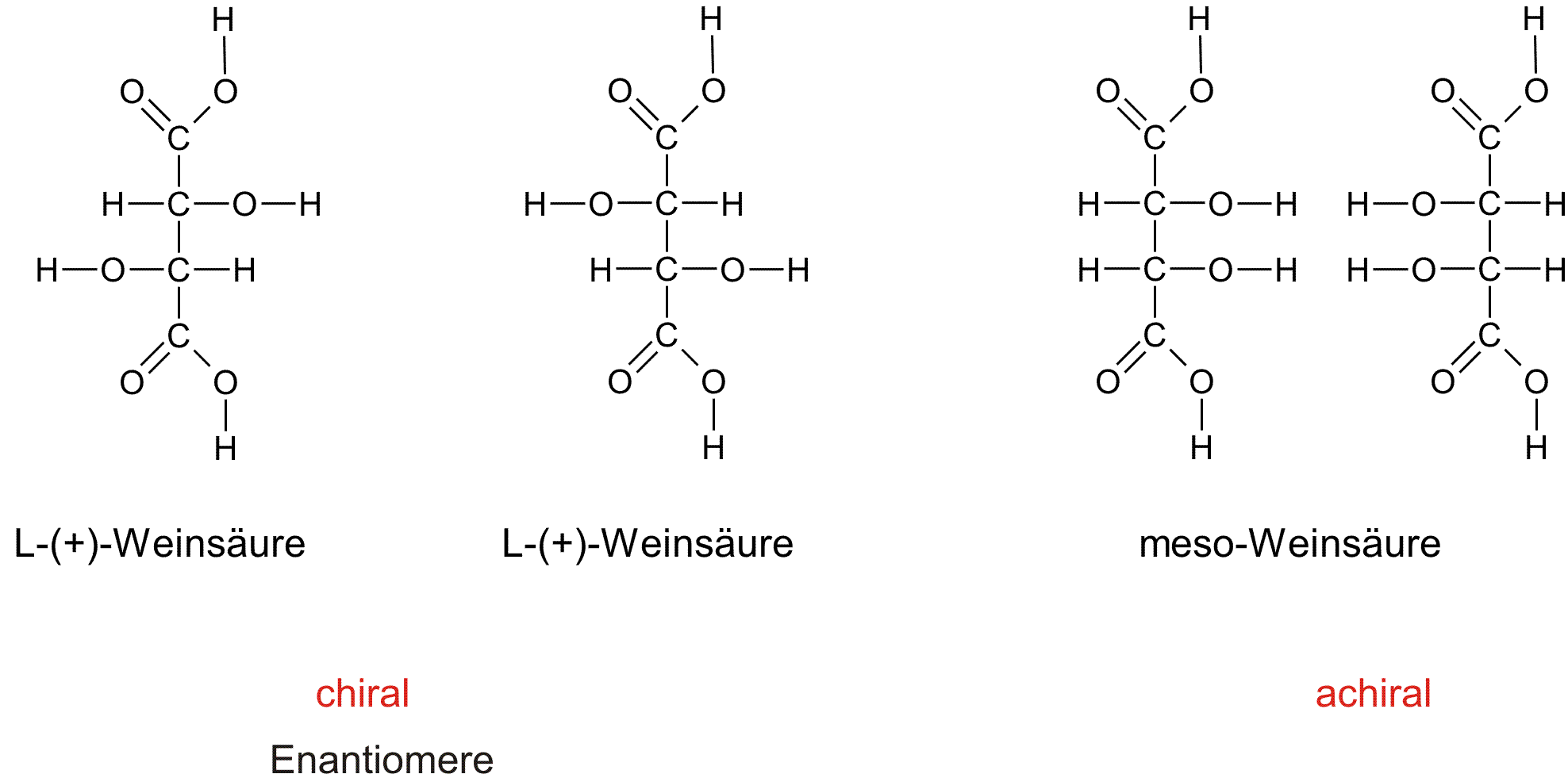
Hat eine Verbindung n asymmetrische C-Atome, so gibt es meist 2n Stereoisomere. Stereoisomere, die keine Enantiomere sind, heißen Diastereomere und haben verschiedene physikalische Eigenschaften.
Substanzen, deren Moleküle mit ihren Spiegelbildern übereinstimmen, obwohl sie Chiralitätszentranen besitzen, heißen meso-Verbindungen ("Das Spiegelbild des Originals kann durch Drehung wieder genau so aussehen, wie das Original). Sie besitzen eine Spiegelebene im Molekül.
-----------------[1] D = dexter (lat) = rechts
[2] L = laevus (lat) = links -
04.1.5 Fructose und Keto-Enol-Tautomerie
4.1.5 Fructose = Fruchtzucker
Vorkommen: in Früchten, Nektar, Honig; vor allem industriell hergestellte Fructose
Eigenschaften: kristallisiert schlecht aus wässriger Lösung → sirupartige Flüssigkeit.
Summenformel: C6H12O6
Fructose ist somit ein Strukturisomer der Glucose.
a) Seliwanow-Probe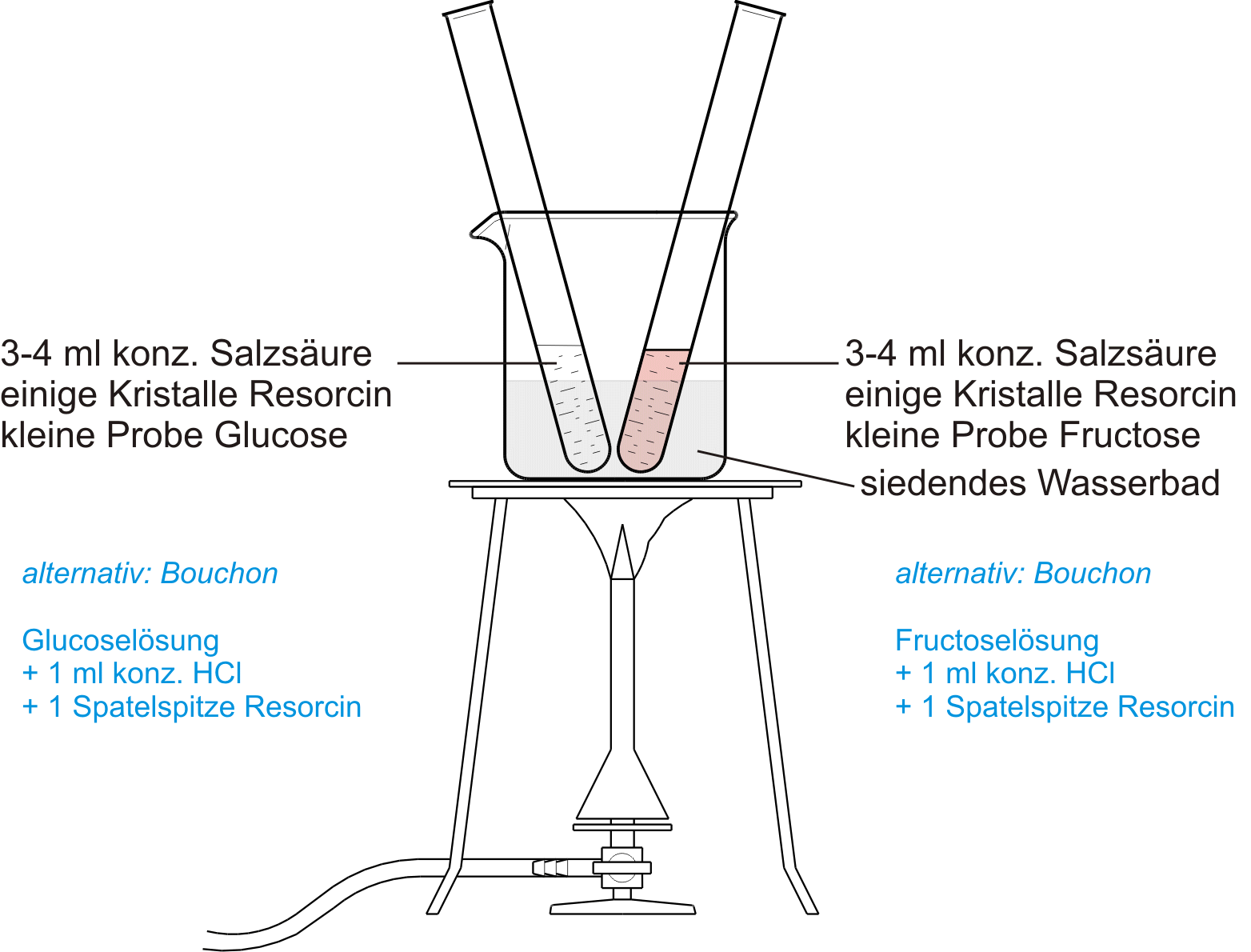
Nachweis, ob es sich bei Kohlenhydraten um Ketosen oder Aldosen handelt.
Ketose --> roter Farbstoff
Aldose --> keine/langsame Reaktion --> farblos
Info: Die Seliwanow-Reaktion ist ein Nachweis für Ketohexosen in der Furanose-Ringform. Da sie im sauren Milieu abläuft, kommt es nicht zur Keto-En(di)ol-Tautomerie. Mit Glucose fällt die Probe deshalb negativ aus.
Strukturformeln: Offenkettige und Ringbildung durch die Halbacetalbildung: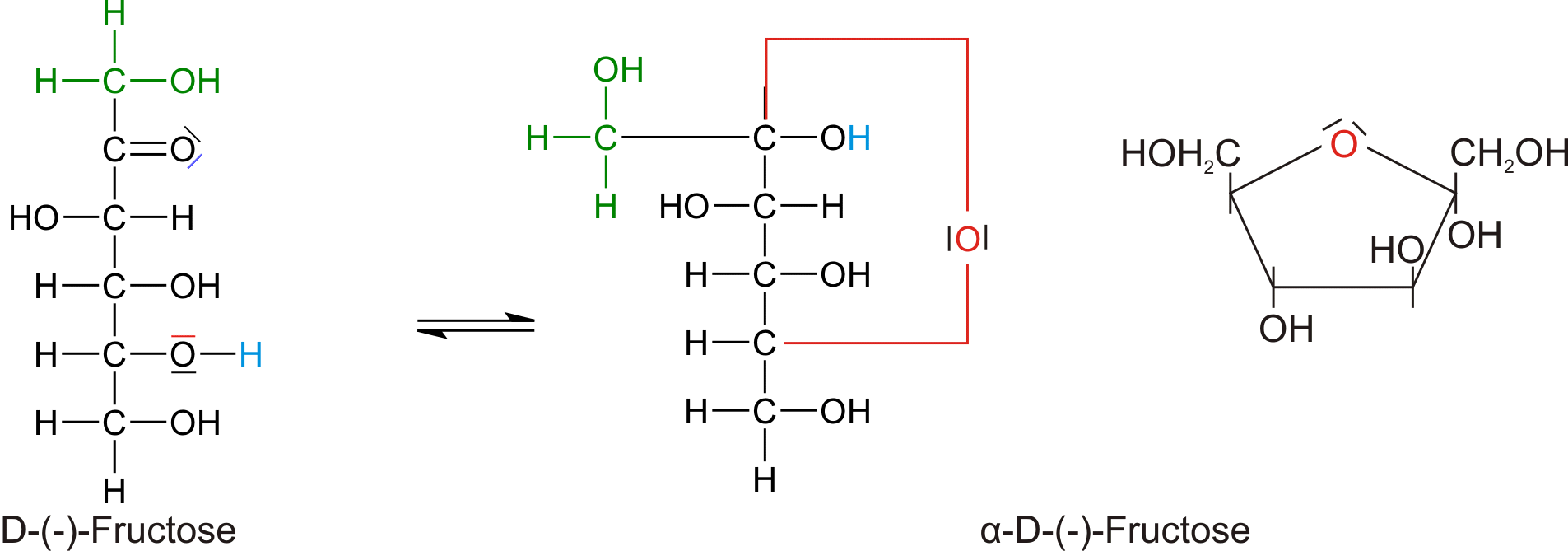
Fructose bildet wie Glucose Anomere. Neben der Kettenform des Moleküls enthält das Gleichgewicht zwei anomere Pyranosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C5-Atom) und zwei anomere Furanosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C6-Atom).
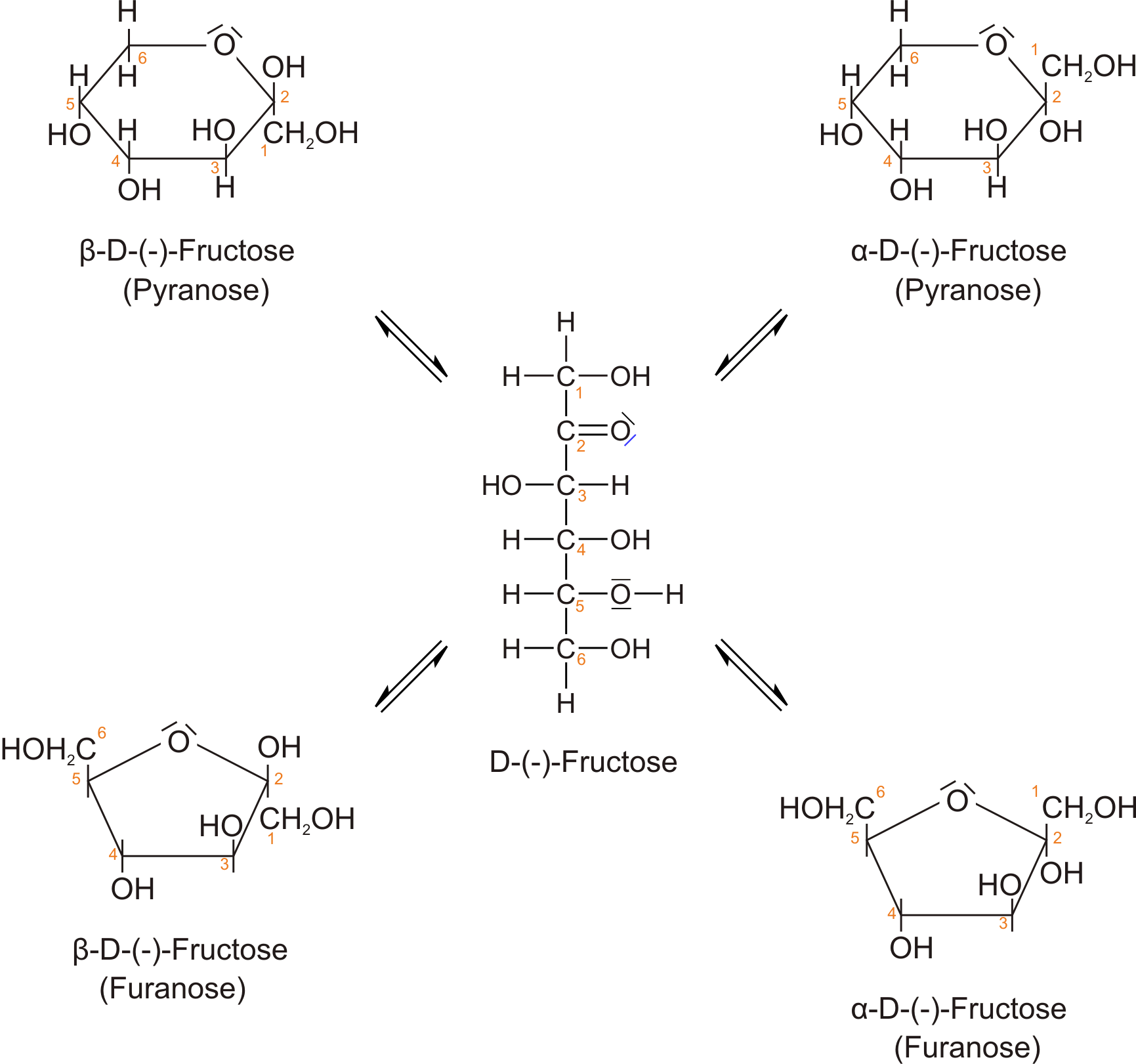
Keto-Enol -Tautomerie
Versuche mit Fructose:- Fehling → positiv
- Tollens → positiv
- GOD (Glucose-Nachweis) + Lauge → positiv
Funktioniert nicht mit einer Ketogruppe, da diese nicht weiter oxidiert werden kann. Grund, warum die Nachweise trotzdem positiv verlaufen: Innermolekulare Umlagerung unter Protonenwanderung und Elektronenverschiebung.
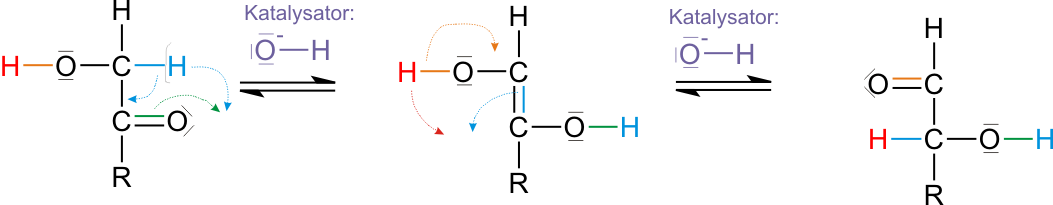
Genauer:
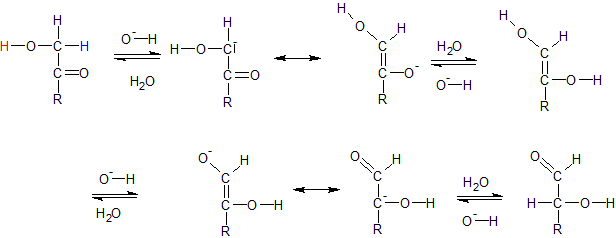
Glucose und Fructose stehen im Gleichgewicht (Glucose überwiegt); bei der Oxidation von Glucose wird Glucose aus dem GG entfernt → Fructose wird aufgebraucht.
-
6.2 Alkanone (Ketone)
6.2 Alkanone (Ketone)
6.2.1 Herstellung von Alkanonen (Ketonen)
Versuch
Die heiße CuO-Spirale wird mehrmals in 2-Propanol getaucht.Beobachtung
Der schwarze Überzug verschwindet; es entsteht blankes Kupfer. Zusätzlich tritt ein charakteristischer Geruch auf.
Zugabe von FSS zur abgekühlten Lösung gibt keine Violettfärbung.Auswertung
Es handelt sich um eine Redoxreaktion. Die Cu²⁺-Ionen werden zu Kupferreduziert und 2-Propanol (Isopropanol) wir zu Propanon (Aceton) oxidiert.Reaktionsgleichung
Versucht einmal für diese Herstellung die Reaktionsgleichung mit Hilfe von Strukturformeln zu formulieren. Wer Hilfen braucht, kann ja ein paar Seiten vorher schauen, wo die primären Alkohole oxidiert wurden.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Merke: Alle sekundären Alkohole lassen sich durch Oxidation (bzw. Dehydrierung) in Ketone (Alkanone) überführen.
6.2.2 Funktionelle Gruppe der Alkanone (Ketone)
Die Alkanone besitzen (auch) eine „Carbonyl-Gruppe“.
Speziell hier: „Keto-Gruppe“6.2.3 Eigenschaften und Verwendung von Aceton (Propanon)
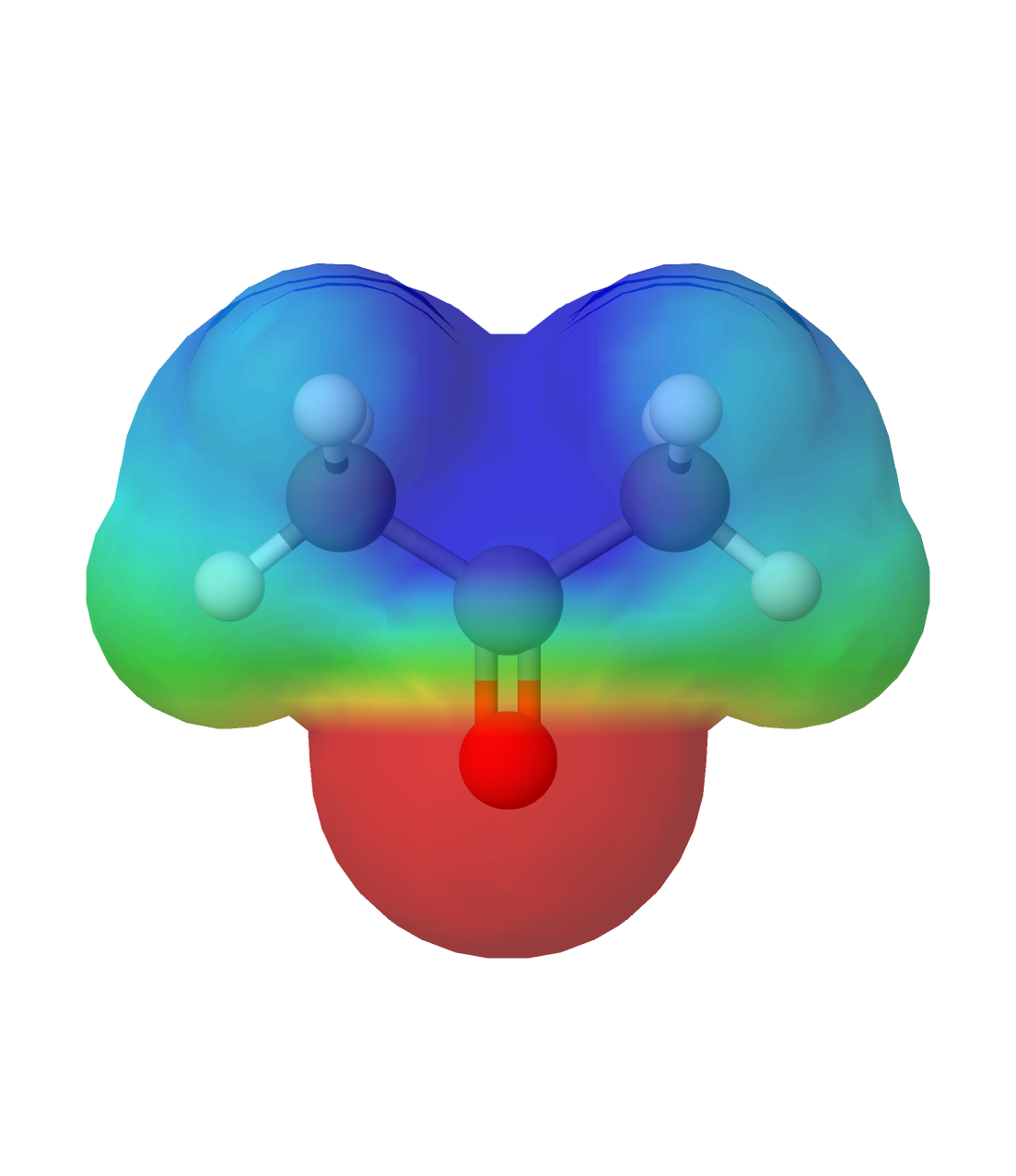
Aceton ist eine farblose, charakteristisch riechende Flüssigkeit (Sdp.: 56 °C). Aceton ist brennbar. Aceton löst sowohl hydrophile (z.B. H₂O, C₂H₅OH ⇨ kann mit diesen Molekülen auch H-Brücken eingehen) als auch hydrophobe Stoffe. ⇨ Verwendung: Lösungsmittel.
Erkennbar, dass Aceton ein gutes Lösungsmittel ist, zeigt die nächste Abbildung. Was dort rot gefärbt ist, zeigt näherungsweise die negative Partialladung (anders als bei meiner Farbgebung) umd den Stauerstoff und was blau gefärbt ist, die positive Partialladung.