Chemie (vom ägyptischen ch'mi = schwarz) ist eine Naturwissenschaft. Sie ist die Lehre von den Stoffen, ihrem Aufbau, ihren Eigenschaften und ihren Reaktionen.
1.1 Körper und Stoff
Körper: Die Gegenstände unserer Umwelt heißen Körper. Jeder Körper hat eine bestimmte Masse und nimmt einen Raum ein.
Stoff: nennt man das Material, aus dem die Körper bestehen.
1.2 Eigenschaften der Stoffe
Stoffeigenschaften lassen sich auf drei Arten erfassen:
a) Mit den Sinnen wahrnehmbar:
Aussehen (Farbe, Oberflächenglanz, Kristallform) · Geruch · Geschmack
b) Mit Geräten messbar:
Elektrische Leitfähigkeit · Schmelztemperatur · Siedetemperatur · Härte
c) Weitere Eigenschaften:
Löslichkeit · Magnetismus · Wärmeleitfähigkeit · Brennbarkeit · Dichte
1.2.1 Dichte und Dichtebestimmung
Die Dichte (Formelzeichen: ρ, griechisch: Rho) ist eine physikalische Eigenschaft eines Materials. Sie ist eine Stoffkonstante — unabhängig vom Ort, aber abhängig von Temperatur und Druck.

a) Dichtebestimmung von Flüssigkeiten
[Schülerexperiment: Dichtebestimmung von Alkohol und Wasser]
Schritt 1: Volumen mit dem Messzylinder ermitteln.
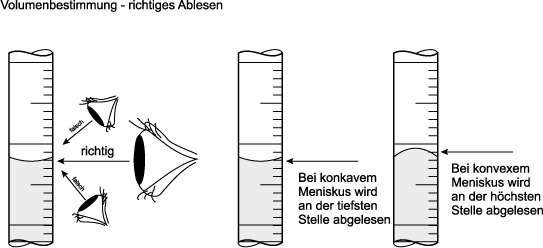
Schritt 2: Masse durch Wägung bestimmen.
Schritt 3: Dichte berechnen (ρ = m ÷ V)
Ergebnis: Dichte von Wasser ≈ 1,00 g/cm³ · Dichte von Ethanol ≈ 0,79 g/cm³
b) Dichtebestimmung von Feststoffen
[Schülerexperiment: Dichtebestimmung von Kupfer und Eisen]
Schritt 1: Masse der Stoffportion bestimmen (Waage)
Schritt 2: Volumen bestimmen (Wasserverdrängung im Messzylinder)
Schritt 3: Dichte berechnen
Ergebnis: Dichte von Kupfer = 8,93 g/cm³ · Dichte von Eisen = 7,87 g/cm³
c) Dichtebestimmung von Gasen

Eine Gaswägekugel wird mit der Wasserstrahlpumpe luftleer gepumpt und gewogen. Mit einem Kolbenprober wird eine Gasportion bekannten Volumens (100 ml) eingefüllt. Die Kugel wird erneut gewogen — aus Massenzunahme und Volumen ergibt sich die Dichte.
Ergebnis: Dichte von Luft bei 20 °C und 1013 hPa ≈ 0,00129 g/cm³
Übungsaufgaben zur Dichte
Klicke auf eine Karte um die Lösung zu sehen — klicke erneut um zurückzublättern.
Chemie Klasse 8 · Stoffe und ihre Eigenschaften · Dichte und Dichtebestimmung · Gymnasium Baden-Württemberg · Bildungsplan 2016
