5.4.3 Polysaccharide
- Wichtigsten Beispiele: Stärke, Glykogen (tier. Stärke), Cellulose
- Funktion: Speicher- und Gerüstsubstanz
- Monomere der genannten Beispiele: Glucose; unterschiedl. Verknüpfung
4.3.1 Stärke
a) Vorkommen:
- Pflanzen (Speicherstoff, osmotisch nicht wirksam)
- Nahrungsmittel (Brot, Teigwaren, Kartoffel, usw.),
b) Aufbau eines Stärkemoleküls:
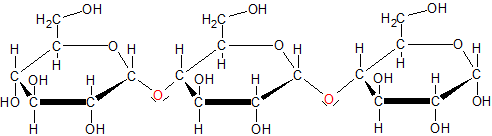
c) Bau: α-D-Glucose – Stärkekorn
| Amyolse | Amylopektin | |
| Anteil: | (10-30%) | (70-90%) |
| Bau: |
linearen Ketten (helikaler (Schrauben-)Struktur) |
stark verzweigten Strukturen |
| Verknüpfung | α-1,4-glykosidisch |
α-1,4-glykosidischen |
| Löslichkeit in heißem Wasser | kolloidal löslich | unlöslich |
| Mit I2 bildet es __ Lösung | blaue | violette |
| Im Stärkekorn | Hülle | Innen |
d) Nachweis: Iodstärke-Reaktion
Versuch: Zu einer Stärkelösung gibt man ein paar Tropfen einer Lösung von Iod in Kaliumiodid (Iod-Kaliumiodid-Lösung, Lugolsche Lösung) Elementares Iod ist in Wasser kaum löslich. Liegen jedoch schon gelöste Iodid-Ionen vor, löst sich das Iod unter Bildung von Polyiodidionen:
2 I2 + I- → I3- + I2 → I5-
Beobachtung: Lösung wird tiefblau
Beim Erhitzen wird die Lösung hell, beim Abkühlen wieder tiefblau
Erklärung: Die Stärkemoleküle sind spiralig angeordnet, in den entstehenden Hohlraum lagern sich Jodmoleküle ein die dort durch van-der-Waals-Kräfte gebunden werden. Eine blaue Iod-Stärke-Einlagerungsverbindung bildet sich. Das gelbe Licht wird absorbiert, die Lösung erscheint blau. Beim Erhitzen nimmt die Beweglichkeit der I2-Moleküle zu, so dass beim Erhitzen eine Entfärbung eintritt.
Eigenschaften von Stärke (Amylose)
- in kaltem Wasser: unlöslich
- heißem Wasser: löslich
- schmeckt nicht süß
- kolloide Lösung (Kolloide: Moleküle oder Aggregate, die sich aus etw. 103 bis 109 Atomen zusammensetzt und in einem Dispersionsmittel verteilt sind).
Versuch:
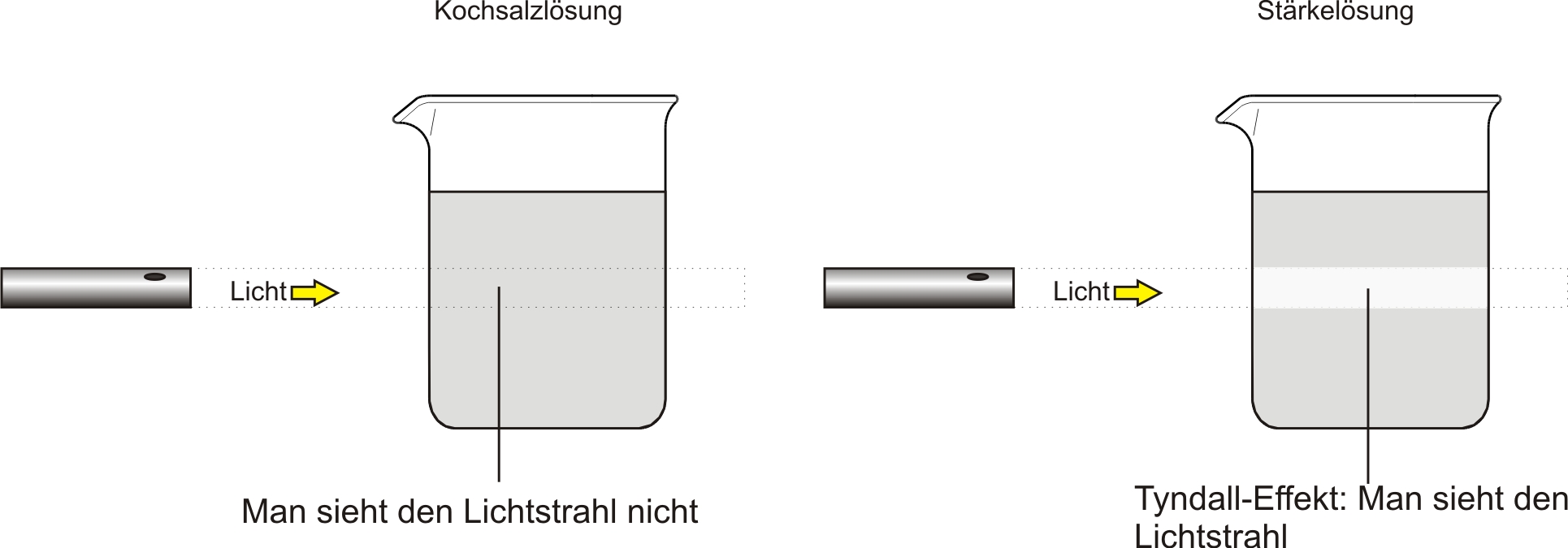
Beobachtung:
Im Gegensatz zu NaCl-Lösung ist der Verlauf des Lichtes in der Stärkelösung sichtbar (= Tyndall-Effekt).
Erklärung:
Gebündeltes Licht wird beim Durchgang durch kolloid- oder molekulardisperse Systeme gestreut (d.H. jedes Teilchen streut einen Teil des auftreffenden Lichtes in alle Richtungen des Raums. Dieser von Tyndall 1868 erstmals untersuchte Effekt tritt immer dann auf, wenn Teilchen vorliegen, deren Größe etwa der Wellenlänge des Lichtes entsprechen. Solche Teilchen haben einen Durchmesser von 1 bis 1000 nm.
van-der-Waals-Kräfte/strong
