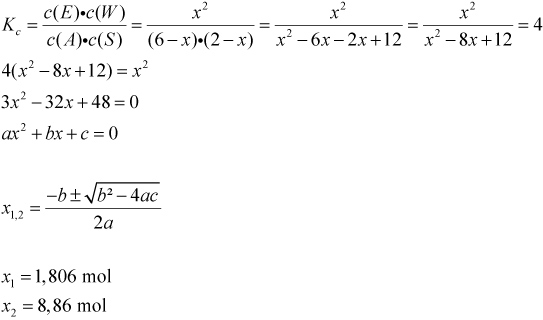2.14 Berechnungen zum Massenwirkungsgesetz
Berechnungen zum Massenwirkungsgesetz können nach folgender Schrittfolge durchgeführt werden:
- Aufstellung der Reaktionsgleichung
- Angeben der Stoffemengenkonzentrationen (Partialdrücke) der Reaktionspartner vor dem Reaktionsbeginn (Start)
- Ermitteln der Stoffmengenkonzentrationen (Partialdrücke) der Reakionsteilnehmer im chemischen Gleichgewicht.
- Aufstellen der Gleichung des Massenwirkungsgesetzes (MWG).
- Einsetzen der Stoffmengenkonzentrationen (Partialdrücke) in die Gleichung des Massenwirkungsgesetzes.
- Berechnung der unbekannten Größe.
Hinweis: Bei chemischen Gleichgewichten mit gleicher Summe der Stöchiometriezahlen der Ausgangsstoffe (Edukte) und der Reaktionsprodukte (Produkte) können anstelle der Stoffmengenkonzentrationen die ihnen proportionalen Stoffmengen eingesetzt werden.
Stoffemengenkonzentration: Quotient aus der Stoffmenge n(B) des gelösten Stoffes B und dem Volumen der Lösung (=Gesamtvolumen nach dem Mischen bzw. lösen).
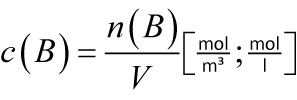
- M(B): Molare Masse des gelösten Stoffes B;
- m(B): Masse des gelösten Stoffes B;
- n(B): Stoffmenge des gelösten Stoffes B
![]()
2.14.1 Berechnung der Gleichgewichtskonzentration
Aufgabe:
Wie viel mol Ester erhält man im GG, wenn man von 6 mol Ethanol und 2 mol Essigsäure (Ethansäure) ausgeht? Angenommen, die GG-Konstante Kc betrüge 4.
Ansatz und Lösung:
Zuerst das Reaktionsschema erstellen;
{slider title="Ansatz und Lösung" open="false" class="icon"}
Ausgangsstoffmenge: 2 mol + 6 mol ⇌ 0 mol + 0 mol
GG-Stoffmenge: (2mol – x) + (6mol – x) ⇌ x mol + x mol
{/sliders}
Das MWG aufstellen und die Werte einsetzen:
{slider title="Ansatz und Lösung" open="false" class="icon"}
Es ist nur der Wert für x1 = 1,806 mol Ester möglich.
{/sliders}
Im GG-Zustand liegen 1,806 mol Ester vor.
2.14.2 Berechnung der Gleichgewichtskonstanten
Aufgabe:
Setzt man 1 mol Ethanol mit 0,5 mol Essigsäure um, so erhält man im GG-Zustand 0,42 mol Essigsäuremethylester. Berechne die GG-Konstante KC.
Ansatz und Lösung:
Zuerst das Reaktionsschema erstellen;
{slider title="Ansatz und Lösung" open="false" class="icon"}

Ausgangsstoffmenge: 0,5 mol + 1 mol ⇌ 0 mol + 0 mol
GG-Stoffmenge: (0,5 mol – 0,42 mol) + (1 mol – 0,42 mol) ⇌ 0,42 mol + 0,42 mol
Das MWG aufstellen und die Werte einsetzen:
![]()
{/sliders}
Ergebnis:
Die GG-Konstante Kc beträgt 3,8.