Aldehyde
-
04.1 Monosaccharide
4.1 Monosaccharide
4.1.1 Glucose - Traubenzucker
Vorkommen: Trauben, Früchte
a) physikalische Eigenschaften- Aggregatzustand: fest; Schmelzpunkt um 146°C; weiteres Erhitzen führt zur Zersetzung.
Folgerung: Glucose besitzt hohe zwischenmolekulare Kräfte (Vermutung: H-Brückenbindung) und van-der-Waals-Kräfte.
- Löslichkeit:
Glucose löst sich sehr gut in Wasser (67g/100ml), dagegen löst sich Glucose nicht in Benzin. Eine wässrige Glucoselösung zeigt (fast) keine elektrische Leitfähigkeit.
Folgerung: Glucose enthält polare Gruppen, die mit Wasser H-Brücken eingehen können. Es entsteht keine Ionen.
b) qualitative Elementaranalyse
Reaktion von Glucose mit konzentrierter Schwefelsäure:
Folgerung: Glucose enthält Kohlenstoff.
Mitteilung: Glucose enthält neben C noch H und O.
c) quantitative Elementaranalyse
Die quantitative Elementaranalyse nach Liebig ergibt:
3,6 g Glucose liefert bei der Verbrennung:- 5,28 g CO2
- 2,16 g H2O
Glucose besitzt folgende Summenformel: CnH2nOn
Von dieser allgemeinen Formel [C(H2O)]n leitet sich die Bezeichnung Kohlenhydrate ab.
Hinweis: Im Heft folgen jetzt die Arbeitsanleitung zur Strukturaufklärung (mit den diversen Experimenten). Hier folgt jedoch gleich das Ergebnis. Die Reaktionsgleichungen von Fehling und Tollens-Reagenz finden sich dann auf anderen Seiten.Ergebnis:
Glucose ist ein Polyhydroxyaldehyd, genauer Pentahydroxyhexanal, ein Aldehydzucker oder Aldose.
Aldose = Monosaccharide, mit terminaler Carbonylgruppe (Aldehyd)
Ketosen = Monosaccharide, mit nicht endständiger Carbonylgruppe (Keton).
Fischerprojektion:
Es gelten folgende Regeln:
- Die C-C-Kette wird senkrecht geschrieben.
- Die am höchsten oxidierte Gruppe steht oben.
- Die C-C-Bindungen sind bei jedem C-Atom nach hinten abgewinkelt;
- dann zeigen die waagrechten Bindungen nach vorne;
- Bei der offenen Glucoseform gibt es vier asymmetrische C-Atome ==> 24-Isomere;
- Die Bezeichnung erfolgt nach dem untersten C-Atom (hier C5-Atom).
- Da die OH-Gruppe rechts steht ==> D-Konfiguration.
- ==> D-(+)-Glucose
(L-Glucose erhält man nur synthetisch)
Bildung von Glucose:
Bei Pflanzen (Fotosynthese) und Tieren (durch Abbau von anderen Molekülen).
Fotosynthese:
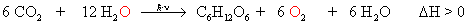
60 Mrd t Kohlenstoff werden dabei im Jahr gebunden.
Abbau von Glucose:
Bei der Zellatmung (Pflanzen, Pilze, Tiere)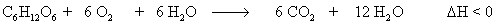
- Aggregatzustand: fest; Schmelzpunkt um 146°C; weiteres Erhitzen führt zur Zersetzung.
-
04.1.2 Halbacetalbildung
4.1.2 Halbacetalbildung bei Zucker (z.B. Glucose)
a) Strukur eines Aldehyds (Alkanals)
Folgende Abbildung zeigt, wie eine Aldehydgruppe angegriffen werden. Durch die höhere Elektronegativität des Sauerstoffatoms werden die Elektronen vom Kohlenstoff weg hin zum Sauerstoff gezogen (polare Atombindung). Dadurch kann am Kohlenstoff ein nucleophiles (kernliebendes Teilchen) angreifen. Nucleophile Teilchen besitzen ein freies Elektronenpaar, mit dem es angreifen kann.Der Sauerstoff der Aldehydgruppe besitzt ein freies Elektronenpaar. Hier kann ein elektrophiles Teilchen (wie z.B. ein H+ (Proton)) angreifen.

Das Aldehydmolekül enthält eine polare Doppelbindung mit freien Elektronenpaaren; Additionsreaktionen sind möglich.b) Aldehyd + Alkohol (AN-Reaktion = nucleophile Addition)

Halbacetale kann man selten isolieren (Ausnahme: Zucker). Ein Halbacetal kann mit Alkohol zu einem Vollacetal weiterreagieren (vgl. Disaccharide).
-
04.1.3 Ringstruktur der Monosaccharide
4.1.3 Ringstruktur der Monosaccharide
Widersprüche:
- Schiffsche Reagenz (typ. Nachweis für Aldehyde) zeigt keine Farbreaktion.
- Drehwinkel in wässriger Lsg. 52,7° statt 112,2°.
- Tollens (1883) schloss daraus, dass Glucose nicht in der offenen Aldehydform vorliegt.
- Die Ursache hierfür ist in der intramolekularen Verknüpfung der Carbonylgruppe mit einer Hydroxylgruppe des gleichen Zuckermoleküls zu suchen. Es kommt also zu einer innermolekularen Halbacetalbildung.

Haworth-Schreibweise- zyklisches Glucose Molekül wird als liegendes Sechseck [Pyranosen] oder Fünfeck [Furanosen] gezeichnet;
- Ringsauerstoffatom findet sich in der rechten hinteren Ecke [Pyranosen] bzw. im hinteren Eck [Furanosen];
- Substituenten, die in der FISCHERprojektion nach links weisen, stehen in der HAWORTH-Projektion oben ["Kommunistenregel"]
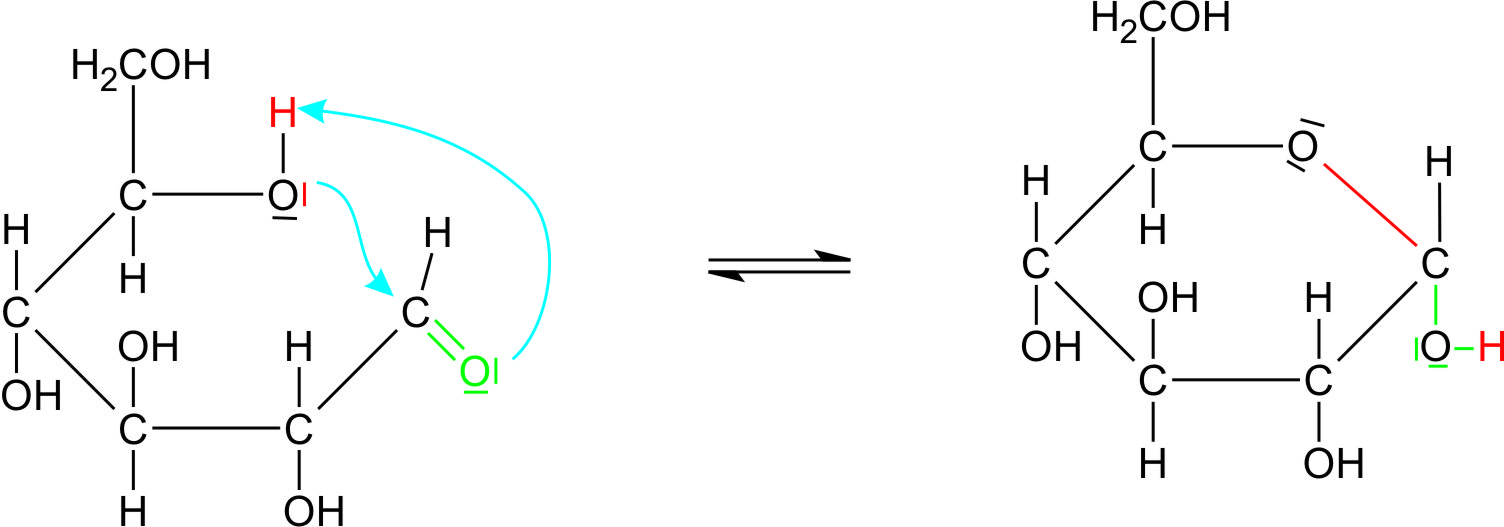
Erklärung der negativen Reaktion der Glucose mit der Schiffschen Reagenz: Es liegt ein Gleichgewicht zwischen der offenen Kette und dem Ring vor, wobei der Anteil der offenen Kette, bei der wirklich ein Aldehyd vorliegt verschwindend gering ist (< 1%):
Aldehydform (offenkettig) ⇌ Halbacetalform (Ring)- Fuchsinschweflige Säure (Schiffsches Reagenz) bildet mit dem Aldehyd eine reversible (umkehrbare) Reaktion, daher findet kein Entzug des Aldehyds statt. Das heißt, es gibt keine GG-Verschiebung und damit keinen wirklichen Aldehydnachweis (der Anteil an offener aldehydhaltigen Glucose ist zu gering).
- Bei der Fehling-Probe und der Tollens-Probe (Silberspiegel) findet eine GG-Verschiebung statt! Die offene Form wird laufend entzogen, neue Ringe gehen auf und es findet langsam der Aldehydnachweis statt.
Durch Ringbildung entstehen 2 Strukturisomere der D-(+)-Glucose (keine Spiegelbildisomere).
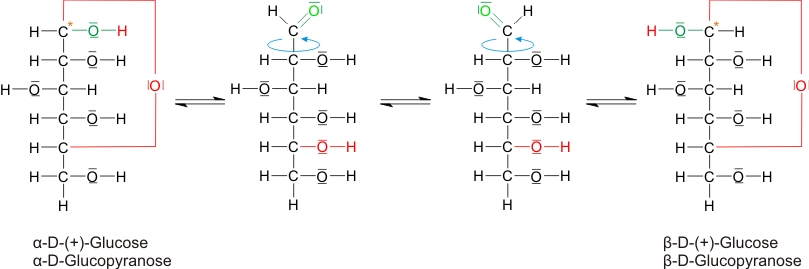
In wässriger Lösung liegen vor:36% 0,26% 64%
Drehwinkel: 112,2° 18,7°
Es entsteht ein neues asymmetrisches C-Atom (= anomeres Kohlenstoffatom) und damit 2 Diasteromere. Anomere = Isomere, die sich nur durch die Stellung der Hydroxylgruppen am anomeren Kohlenstoffatom unterscheiden.
α-Form: OH-Gruppe am neuen asymmetrischen C-Atom liegt auf derselben Seite wie die am untersten asymmetrischen C-Atom.
Muta1rotation: Drehwinkel einer Lösung einer optisch aktiven Substanz ändert sich vom Zeitpunkt des Ansetzens der Lösung kontinuierlich bis zum Erreichen eines festen Wertes. Grund dafür ist, dass man z.B. α-Glucose in eine wässrige Lösung gibt. Sobald sich das Molekül in Wasser löst, öffnen sich einige wenige Moleküle. Bei der erneuten Ringbildung, bildet sich auch β-Glucose. Erst wenn sich der Anteil wie oben angegeben einstellt, ändert sich der Drehwinkel nicht mehr.Glucose α-Form ⇌ offene Form ⇌ β-Form
Bei Glucose ist der Endwert: 0,36 * 112,2° + 0,64 * 18,7° = 52,36°
Haworth-Schreibweise
Achtet auf die Durchnummerierung der C-Atome. Am C1 war ursprünglich die Aldehydgruppe.
α-D-Glucose β-D-Glucose
Nachweis von Glucose: GOD-Test (Glucose-Oxidase-Stäbchen); Achtung beim schriftlichen Abitur: Fehling oder Tollens ist kein Nachweis für Glucose, sondern nur für Aldehydgruppen!- Glucose-Oxidase = Enzym: Oxidiert Glucose am C1-Atom zu Gluconsäure und Wasserstoffperoxid (H2O2).
- Durch das Enzym Peroxidase (z.B. aus Meerettich) wird das Wasserstoffperoxid zu Wasser reduziert.
- je mehr Glucose, umso intensiver die Farbe.
Im Handel als Teststreifen für Diabeteserkrankung.
-----
-
04.1.4 Systematik der Namensgebung
4.1.4 Systematik der Namensgebung einfacher Zucker
a.) nach Anzahl der C-Atome:
- Triosen (3 Cs)
- Tetrosen (4 Cs)
- Pentosen
- Hexosen
- Heptosen
b) nach der funktionellen Gruppe:
Aldosen: enthalten eine Aldehydgruppe
Ketosen: enthält eine Ketogruppe

c) Nach der Größe des Rings in der Ringstruktur
Furanosen: 5er-Ring leitet sich ab von Furan
Pyranosen: 6er-Ring leitet sich ab von Pyran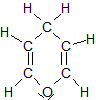
-
04.1.5 Fructose und Keto-Enol-Tautomerie
4.1.5 Fructose = Fruchtzucker
Vorkommen: in Früchten, Nektar, Honig; vor allem industriell hergestellte Fructose
Eigenschaften: kristallisiert schlecht aus wässriger Lösung → sirupartige Flüssigkeit.
Summenformel: C6H12O6
Fructose ist somit ein Strukturisomer der Glucose.
a) Seliwanow-Probe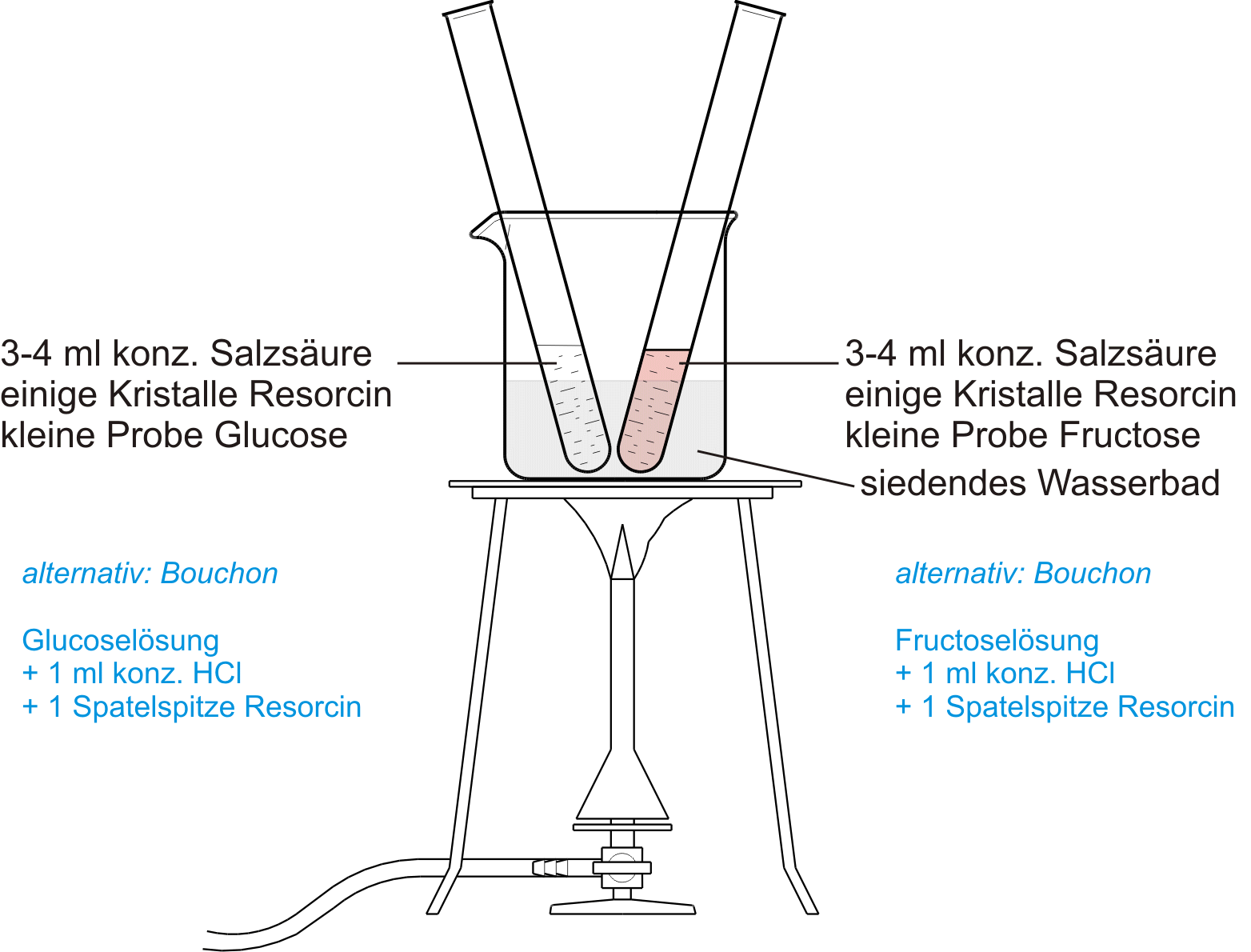
Nachweis, ob es sich bei Kohlenhydraten um Ketosen oder Aldosen handelt.
Ketose --> roter Farbstoff
Aldose --> keine/langsame Reaktion --> farblos
Info: Die Seliwanow-Reaktion ist ein Nachweis für Ketohexosen in der Furanose-Ringform. Da sie im sauren Milieu abläuft, kommt es nicht zur Keto-En(di)ol-Tautomerie. Mit Glucose fällt die Probe deshalb negativ aus.
Strukturformeln: Offenkettige und Ringbildung durch die Halbacetalbildung: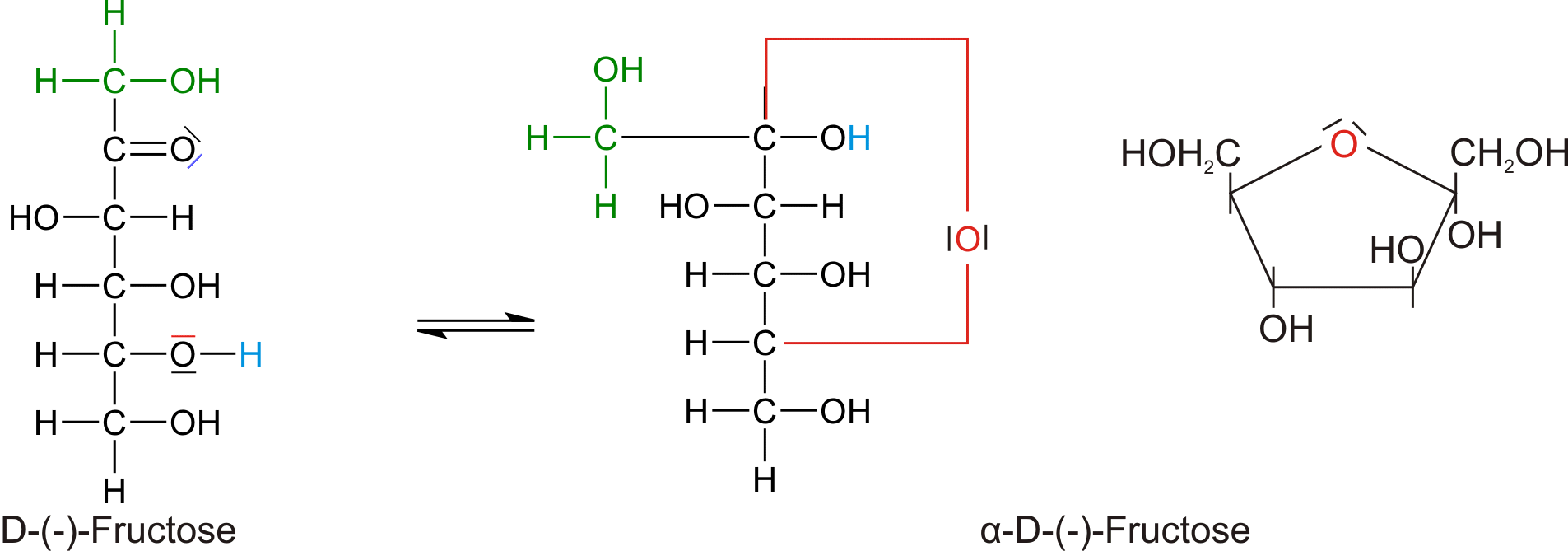
Fructose bildet wie Glucose Anomere. Neben der Kettenform des Moleküls enthält das Gleichgewicht zwei anomere Pyranosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C5-Atom) und zwei anomere Furanosen ( β-D-Fructose und α-D-Fructose; Halbacetalbildung mit dem C6-Atom).
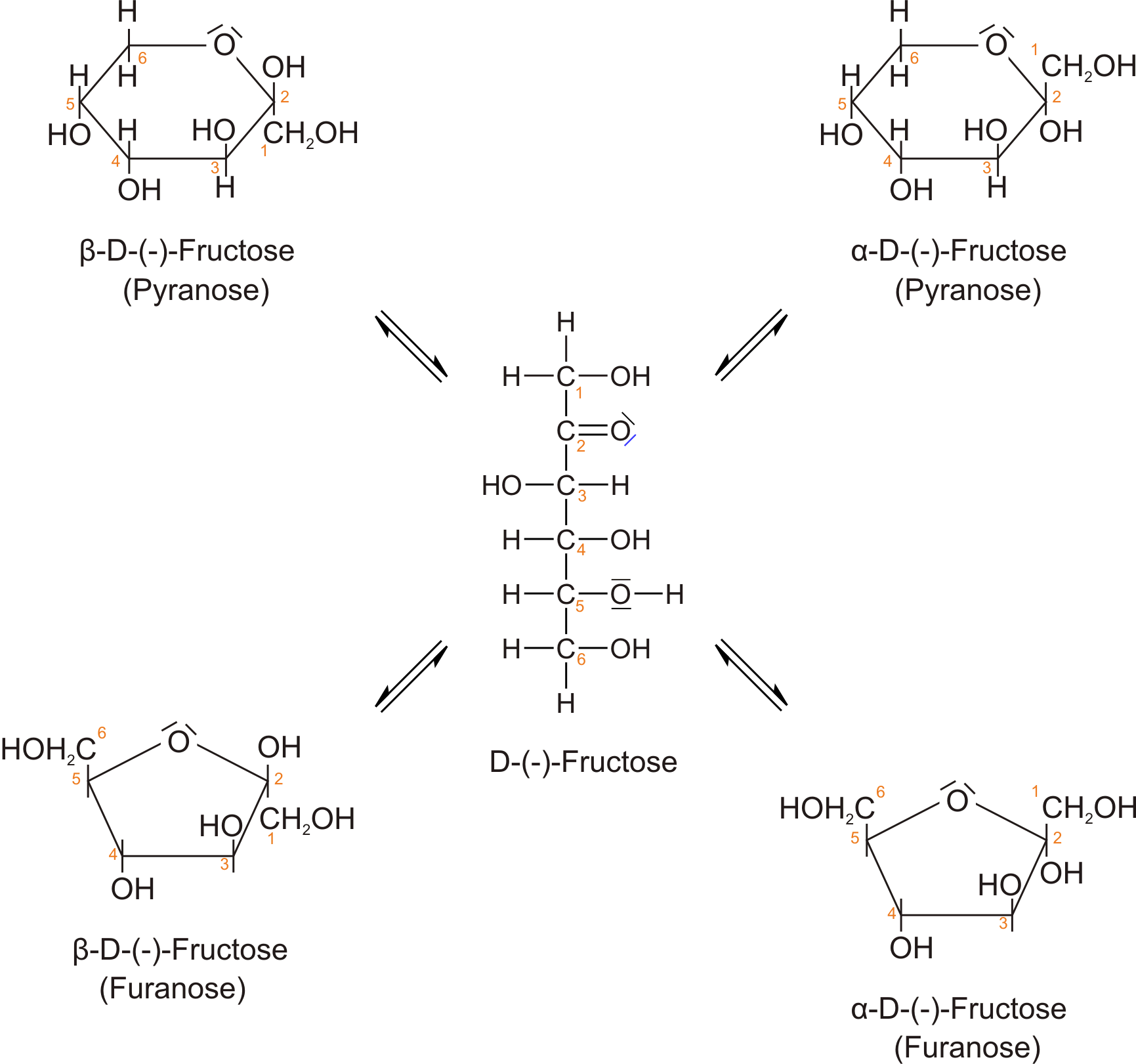
Keto-Enol -Tautomerie
Versuche mit Fructose:- Fehling → positiv
- Tollens → positiv
- GOD (Glucose-Nachweis) + Lauge → positiv
Funktioniert nicht mit einer Ketogruppe, da diese nicht weiter oxidiert werden kann. Grund, warum die Nachweise trotzdem positiv verlaufen: Innermolekulare Umlagerung unter Protonenwanderung und Elektronenverschiebung.
Genauer:
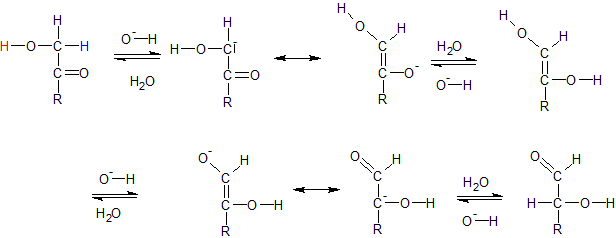
Glucose und Fructose stehen im Gleichgewicht (Glucose überwiegt); bei der Oxidation von Glucose wird Glucose aus dem GG entfernt → Fructose wird aufgebraucht.
-
04.1.7 Glycosid- bzw. Vollacetalbildung
zu 4.1.7 Reaktionen der Monosaccharide
Glycosidbildung (~Halbacetal, Vollacetal)
a) Aldehyd + Alkohol ⇌ Halbacetal (nucleophile Addition)
b) Halbacetal + Alkohol ⇌ (Voll)Acetal + WasserTypische Kondensationsreaktion (unter Wasserabspaltung)
Beispiel:
β-D-Glucose + Methanol ⇌ β-Methyl-Glucosid + Wasser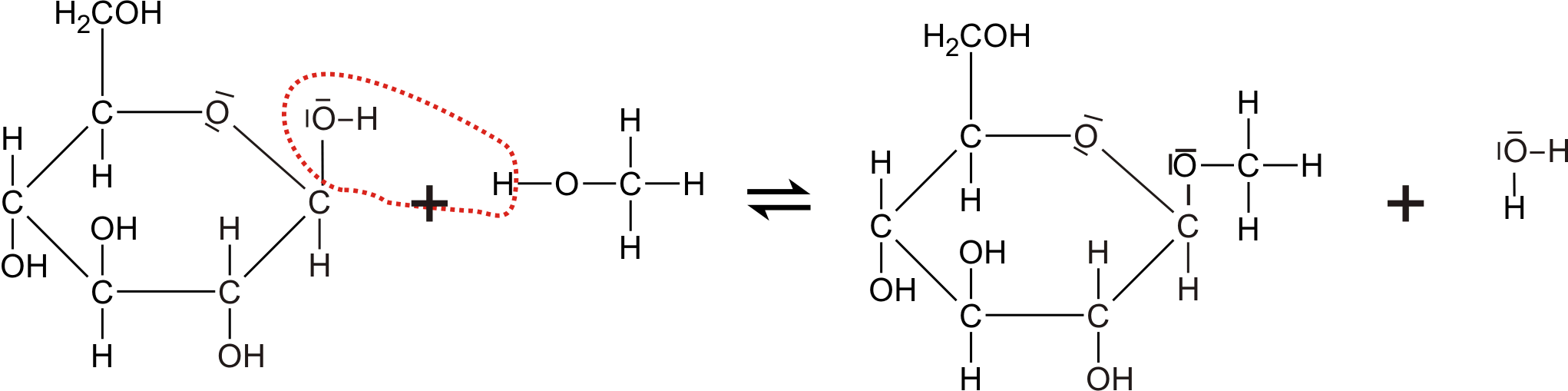
Zucker + Alkohol ⇌ Glycosid + Wasser
Fructose + Alkohol ⇌ Fructosid + Wasser
Glucose + Alkohol ⇌ Glucosid + Wasser
Reaktionen von Zuckern untereinander ergeben Di-, Oligo- und Polysaccharide. -
04.1.7 Reaktionen der Monosaccharide
4.1.6 Galactose = Schleimzucker
Unterscheidet sich von der Glucose durch die Stellung der Hydroxylgruppe am dritten asymmetrischen C-Atom. Kommt in den Schleimhäuten vor (Name!).
4.1.7 Reaktion der Monosaccharide
a) Oxidation zu Polyhydroxysäuren
Bei gelinder Oxidation der Aldosen geht nur die Aldehydgruppe in die Carboxylgruppe über. Durch stärkere Oxidation der Aldosen (z.B. mit konz. HNO3) wird nicht nur die Aldehyd- sondern auch die primäre Alkoholgruppe in die Carboxylgruppe überführt.
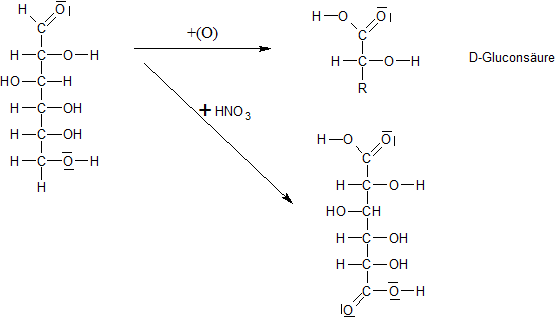
b) Reduktion zu Zuckeralkoholen
Die Monosaccharide lassen sich z.B. katalytisch mit Wasserstoff zu mehrwertigen Alkoholen reduzieren.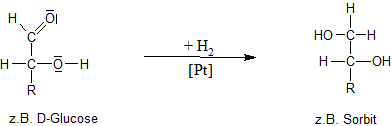
-
6.1.1 Herstellung von Alkanale
6 Carbonylverbindungen – Alkanale (Aldehyde) und Alkanone (Ketone)
6.1 Alkanale (Aldehyde)
6.1.1 Herstellung
Die grundsätzliche Reaktion für die Herstellung ist die Oxidation eines Alkohols. Wichtig dafür ist, dass man die Erlenmeyer-Regel verstanden hat.
Experiment (Hinweis: Anders als bei den Übungen angegeben, darf man den Versuch nicht mit allen Alkanole durchführen, weil extrem giftige Stoffe entstehen können!).
Um einen Alkohol oxidieren zu können, braucht man ein "Oxidationsmittel", also ein Stoff, der andere Stoffe oxidiert. In unserem Schullabor ist das Kupfer(II)-oxid. Dieses Kupfer(II)-oxid stellen wir ganz einfach her, indem wir Kupferblech in einer Teclu-Flamme oxidieren (linke Seite der Abbildung). Dadurch färbt sich das Kupferblechdurch das Kupfer(II)-oxid schwarz.
Übung: Formuliere für diesen Vorgang die Reaktionsgleichung (Struktur- und Summenformel), bestimme die Oxidationszahlen und beurteile welche Atome oxidiert und welche reduziert wurden.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Im nächsten Schritt taucht man noch das heiße, schwarze Kupferblech mit dem Kupfer(II)-oxidschicht in den Alkohol. sofort wird das schwarze Kupfer(II)-oxidblech an den Stellen die in den Alkohol eintauchen blank und kupferfarben. Das Kupfer(II)-Oxid wurd also wieder zu Kupfer reduziert.
Wenn Kupfer reduziert wurde, muss der Alkohol oxidiert werden. In der folgenden Reaktionsgleichung ist das einmal für das Beispiel Methanol dargestellt:
Beispiel Herstellung von Methanal:
I.) Methanol → Methanal
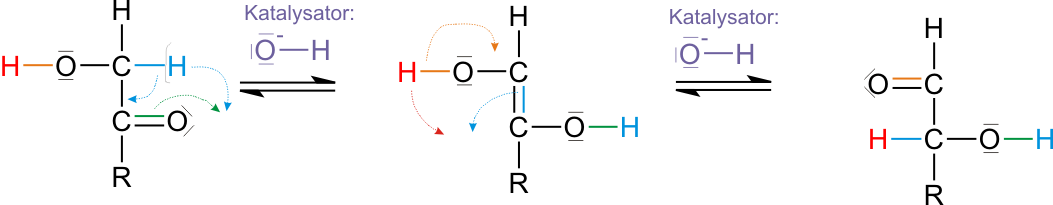
Bei der Reaktion wird Methanol so oxidiert, dass als man sich vorstellen kann, wie zwei Hydroxy-Gruppen an einem C-Atom gebunden werden (Abbildung in der "Wolke"). Dafür wurde zwischen C und H ein Sauerstoff gebunden. Laut Erlenmeyer-Regel geht das aber nicht. Im nächsten Schritt muss also Wasser abgespalten werden und es bildet sich eine Carbonyl-Gruppe, nämlich das Methanal.
Versucht bitte einmal diese Schritte nachzuvollziehen, ich habe sie farbig auch hervorgehoben.
Nun seid ihr dran: Formuliert für die Bildung von Ethanal (aus Ethanol) und Propanal (aus Propanol) auch die Reaktionsgleichungen wie oben.
II) Ethanol → Ethanal
Formuliert für die Bildung von Ethanal aus Ethanol die Reaktionsgleichung mit freien und bindenden Elektronenpaaren.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
III) Propanol → Propanal
Formuliert für die Bildung von Propanal aus Propanol die Reaktionsgleichung mit freien und bindenden Elektronenpaaren.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Wichtig: Alle primären Alkohole lassen sich durch Oxidation (bzw. Dehydrierung) in Aldehyde (Alkanale) überführen.
-
6.1.4 Aldehydnachweise
6.1.4 Aldehydnachweise
a) Schiffsche-Probe mit Fuchsinschwefliger Säure
Fuchsinschweflige Säure ergibt mit Aldehyden eine rotviolette Farbe. Dieser Aldehydnachweis beruht nicht auf der Reduktionswirkung von Aldehyden!
b) Tollens-Probe (Silberspiegel)
Versuchsaufbau (gilt auch für Fehling-Probe)
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.
- Gib in das RG etwa zwei fingerbreit Silbernitratlösung.
- Füge mit der Pipette tropfenweise verdünnte Ammoniaklösung hinzu, bis sich der entstehende Niederschlag gerade wieder auflöst.
- Gib nun in das RG zwei fingerbreit Probelösung.
- Stelle das RG in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein Silberspiegel auf der Innenseite des Reagenzglas.
Auswertung:
Es bedeutet, dass sich die Silber-Ionen zu elementarem Silber reduzierthaben. Da eine Reduktion nur zusammen mit einer Oxidationablaufen, muss etwas anderes oxidiert worden sein. Da es ein Aldehyd-Nachweisist, kann man davon ausgehen, dass das C-Atom der Aldehyd-Gruppe oxidiertwurde. Da diese Reaktion in alkalischer Lösung abläuft (Ammoniak wurde dazugegeben), formuliert man mit Hilfe von Hydroxid-Ionen (OH⁻).
c) Fehling-Reagenz
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.- Gib in das RG etwa 5 ml Fehling 1-Lösung und dann 5 ml Fehling 2-Lösung.
- Füge ein Spatellöffel Glucose zu.
- Stelle das RG nach kurzem Schütteln in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein roter Niederschlag von Kupfer(I)-Oxid (Cu₂O).Auswertung:
Diese Reaktion verläuft recht analog zum Silberspiegel (Tollens-Reagens). Nur wird hierbei das Metall-Ion nicht komplett reduziert, sondern das Cu²⁺ wird zu Cu¹⁺ reduziert, wobei es sich sofort mit einem Oxid-Ion verbindet und den rötlichen Niederschlag bildet. Sauerstofflieferant ist auch in diesem Fall wie bei Tollens-Probe das Hydroxid-Ionen, da eine alkalische Lösung vorliegt.
Aufgabe: Versucht mit Hilfe der oberen Gleichung jetzt die Reaktionsgleichungen für das Fehlingreagenz zu formulieren.
{slider title="Lösung" open="false" class="icon"}
{/sliders}








