Was du auf dieser Seite lernst
Wie lässt sich die Stärke einer Säure quantitativ erfassen? Die Säurekonstante KS beschreibt das Gleichgewicht der Protolyse mit Wasser. Weil die Zahlenwerte sehr klein werden können, rechnet man meist mit dem pKS-Wert: Je kleiner er ist, desto stärker die Säure.
Grundlagen aus Kapitel 3
Die Faktoren für die Säurestärke (Elektronegativität, Atomgröße, –I-Effekt, Mesomerie) kennst du bereits aus dem vorherigen Kapitel: → 3.5 Stärke von Säuren und Basen · → 3.4 Mehrprotonige Säuren
4 Stärke von Säuren und Basen: KS- und KB-Werte
4.1 Säurestärke: der pKS-Wert
Als Maß für die Stärke einer Säure dient das Ausmaß ihrer Reaktion mit Wasser.
Allgemeines Beispiel:
| HA | + | H₂O | ⇌ | A⁻ | + | H₃O⁺ |
| Säure | Base | konj. Base | konj. Säure |
↑ Zum Vergrößern klicken
✕
Wie beim Ionenprodukt des Wassers kann man die Konzentration des Wassers als konstant ansehen und mit der Konstanten K zusammenfassen.
↑ Zum Vergrößern klicken
✕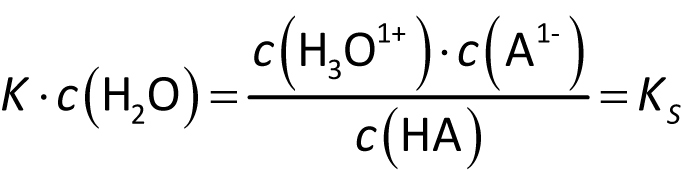
KS ist die Säurekonstante (Säuredissoziationskonstante).
Ist der Zahlenwert von KS sehr groß, so handelt es sich um eine sehr starke Säure.
Folgende Säuren protolysieren in Wasser nahezu vollständig:
- Perchlorsäure HClO₄
- Jodwasserstoff HI
- Chlorwasserstoff HCl
- Schwefelsäure H₂SO₄
⇨ Bei diesen Säuren kann man keinen sinnvollen KS-Wert angeben – das Gleichgewicht liegt nahezu vollständig auf der rechten Seite:
↑ Zum Vergrößern klicken
✕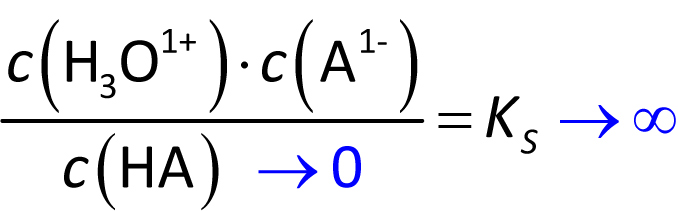
Da die KS-Werte schwacher Säuren sehr klein sind, gibt man die Säurestärke durch den pKS-Wert an:
Es gilt:
↑ Zum Vergrößern klicken
✕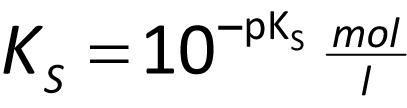
| Kategorie | pKS-Bereich | KS-Bereich | Beispiele |
|---|---|---|---|
| Sehr starke Säuren | pKS < −1 | KS > 10 | HCl, H₂SO₄, HI, HClO₄ |
| Starke Säuren | −1 ≤ pKS < 3,5 | KS zwischen 10 und 3 · 10⁻⁴ | HNO₃, HF (pKS = 3,17) |
| Schwache Säuren | pKS ≥ 3,5 | KS < 3 · 10⁻⁴ | CH₃COOH (4,75), H₂CO₃ (6,35), H₂O (15,74) |
Auf einen Blick – die wichtigsten Aussagen
Definition KS
Die Säurekonstante KS = [A⁻]·[H₃O⁺] / [HA] beschreibt, wie weit das Protolysegleichgewicht auf der rechten Seite liegt. Je größer KS, desto stärker die Säure.
Definition pKS
pKS = −lg(KS). Da KS schwacher Säuren sehr kleine Zahlen sind (z. B. 1,8 · 10⁻⁵), ist der pKS-Wert handlicher: Essigsäure pKS = 4,75.
Sehr starke Säuren
HCl, H₂SO₄, HI, HClO₄ protolysieren in Wasser nahezu vollständig. Das Gleichgewicht liegt so weit rechts, dass kein sinnvoller KS-Wert messbar ist (pKS < −1).
Klassifikation
pKS < −1: sehr stark · −1 bis 3,5: stark · > 3,5: schwach. Kleiner pKS = stärkere Säure. Das gilt auch für mehrprotonige Säuren je Stufe.
Häufige Fragen – KS- und pKS-Wert
Was ist die Säurekonstante KS und wie wird sie berechnet?
Die Säurekonstante KS ist die Gleichgewichtskonstante der Protolyse: KS = [A⁻] · [H₃O⁺] / [HA]. Die Konzentration des Wassers wird dabei als konstant angesehen und in KS einbezogen. Je größer KS, desto weiter liegt das Gleichgewicht auf der rechten Seite – und desto stärker die Säure. Für Essigsäure gilt: KS = 1,8 · 10⁻⁵ mol/L.
Warum kann man für sehr starke Säuren keinen KS-Wert angeben?
Bei sehr starken Säuren wie HCl oder H₂SO₄ ist das Protolysegleichgewicht nahezu vollständig auf die rechte Seite verschoben. Die Konzentration der undissoziierten Säure [HA] geht gegen null – der Nenner im KS-Ausdruck wird so klein, dass kein sinnvoller Wert messbar ist. Man spricht von vollständiger Protolyse. Der pKS-Wert ist für diese Säuren negativ (pKS < −1).
Was bedeutet pKS = −lg(KS) praktisch?
Der pKS-Wert ist der negative Zehner-Logarithmus der Säurekonstanten. Er macht es einfacher, sehr kleine Zahlen zu vergleichen: KS = 1,8 · 10⁻⁵ wird zu pKS = 4,74. Merke: 1 Einheit pKS-Unterschied entspricht einer Faktor-10-Differenz in der Säurestärke. Außerdem gilt: KS = 10−pKS.
Wie unterscheidet man starke von schwachen Säuren anhand des pKS-Werts?
Die Grenze liegt bei pKS ≈ 3,5: Säuren mit pKS < 3,5 gelten als stark (z. B. HF: 3,17), Säuren mit pKS > 3,5 als schwach (z. B. Essigsäure: 4,75, Kohlensäure: 6,35). Schwache Säuren liegen im Gleichgewicht größtenteils als undissoziierte Moleküle vor – nur ein kleiner Bruchteil gibt ein Proton ab. Mehr dazu im Abschnitt über den → pH-Wert.
Wie berechnet man den pH-Wert einer schwachen Säure über KS?
Für eine schwache Säure HA mit der Anfangskonzentration c₀ gilt näherungsweise: [H₃O⁺] ≈ √(KS · c₀). Damit ergibt sich pH = −lg[H₃O⁺] = ½ · (pKS − lg c₀). Für Essigsäure mit c₀ = 0,1 mol/L und pKS = 4,75: pH = ½ · (4,75 − (−1)) = ½ · 5,75 ≈ 2,87. Das stimmt gut mit dem gemessenen Wert von pH = 2,9 überein (vgl. → Kap. 3.6).
Lernkarten – KS- und pKS-Wert
Klicke auf eine Karte, um die Antwort zu sehen.
Schreibe den Ausdruck für KS der Reaktion HA + H₂O ⇌ A⁻ + H₃O⁺.
KS = [A⁻] · [H₃O⁺] / [HA]
Die Konzentration des Wassers ist konstant und wird in KS eingerechnet.
Essigsäure: KS = 1,8 · 10⁻⁵ mol/L. Berechne pKS.
pKS = −lg(1,8 · 10⁻⁵)
= −(lg 1,8 + lg 10⁻⁵)
= −(0,26 − 5)
= 4,74
Ordne zu: pKS < −1 / −1 bis 3,5 / > 3,5 → sehr stark / stark / schwach.
pKS < −1 → sehr starke Säure (HCl, H₂SO₄)
−1 ≤ pKS < 3,5 → starke Säure (HF, HNO₃)
pKS ≥ 3,5 → schwache Säure (CH₃COOH, H₂CO₃)
Warum können für HCl und H₂SO₄ keine KS-Werte angegeben werden?
Beide Säuren protolysieren nahezu vollständig. [HA] → 0, der Nenner im KS-Ausdruck geht gegen null – kein messbarer Wert möglich. Das Gleichgewicht liegt praktisch vollständig auf der rechten Seite.
Berechne näherungsweise den pH-Wert von Essigsäure (c₀ = 0,1 mol/L, pKS = 4,75).
Näherung: pH ≈ ½ · (pKS − lg c₀)
= ½ · (4,75 − lg 0,1)
= ½ · (4,75 + 1)
= ½ · 5,75
≈ 2,88
Weiter im Kapitel Säure-Base-Reaktionen
← 3.5/3.6 Säurestärke und Molekülstruktur → pH-Wert → Pufferlösungen
🔁 Verwandt: Mehrprotonige Säuren – pKS-Werte je Stufe (3.4)
