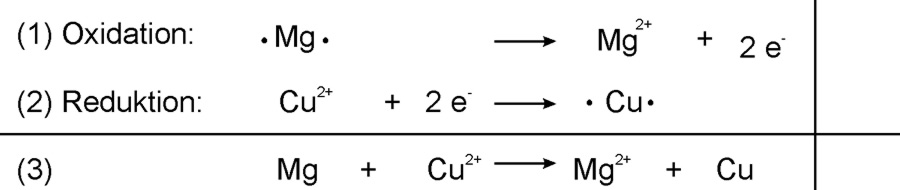Reduktionsmittel
-
1 Freiwillig ablaufende Reaktionen
Was du auf dieser Seite lernst
Du wiederholst die Grundbegriffe der Redoxchemie und lernst sie neu zu durchdenken: Was bedeuten Oxidation und Reduktion im Sinne der Elektronenübertragung? Was ist ein korrespondierendes Redoxpaar? Am Beispiel Magnesium + Sauerstoff werden Reaktionsgleichung, Redoxschema und Elektronenbilanz erarbeitet.
Grundlagen aus der 9. Klasse
Den Versuch Magnesium + Sauerstoff und die erste Einführung in Oxidation und Reduktion kennst du bereits aus der 9. Klasse: → Magnesium und Sauerstoff (Kl. 9) · → Neue Definitionen: Oxidation / Reduktion (Kl. 9)
1.1 Wiederholung bekannter Begriffe und Definitionen
Versuch 1: Magnesium + Sauerstoff
Magnesium verbrennt mit stark leuchtender Flamme. Ein weißer Feststoff bleibt übrig.
Formuliere die Reaktionsgleichungen und ein Redoxschema:
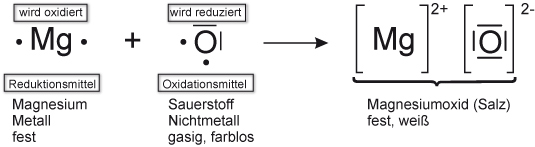
✕Lösung: Reaktionsgleichung und Redoxschema Mg + O₂
Zunächst vereinfacht atomar (natürlich liegt Sauerstoff molekular vor):
↑ Zum Vergrößern klicken
Vollständiger:
Reaktionsgleichung: 2 Mg + O2 → 2 MgO ΔH < 0
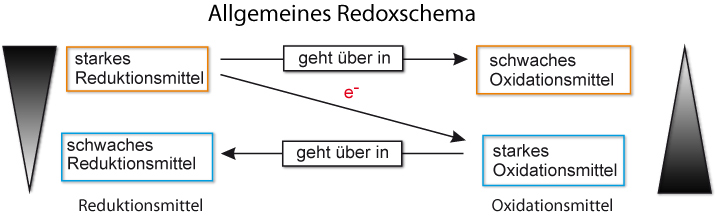
Redoxschema (allgemein):
↑ Zum Vergrößern klicken
↑ Zum Vergrößern klicken
 ✕
✕
 ✕
✕
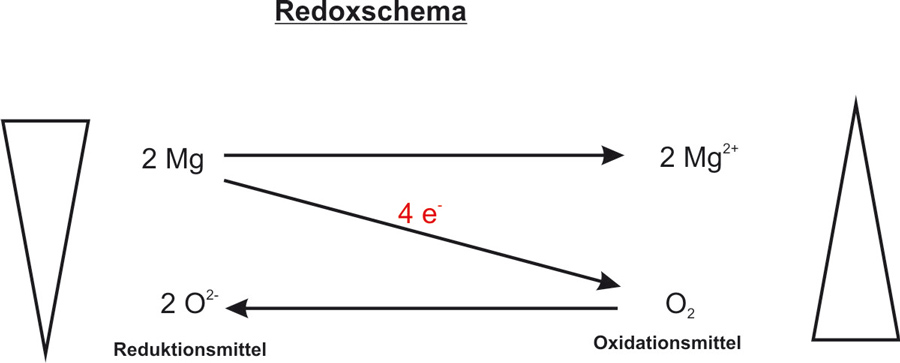
Einfach ist es, wenn man die Teilreaktionen (Oxidation und Reduktion) erstellt und dann erst die Redoxreaktion. Versucht mal diese zu formulieren:
Lösung: Teilreaktionen und Elektronenbilanz Mg + O₂
Oxidation: Mg → Mg2+ + 2 e− | · 2
Reduktion: O2 + 4 e− → 2 O2− | · 1
————————————————————————
Redoxreaktion: 2 Mg + O2 → 2 Mg2+ + 2 O2−Begriffe und Definitionen
Oxidation = Elektronenabgabe; Erhöhung der Oxidationszahlen
Reduktion = Elektronenaufnahme; Erniedrigung der OxidationszahlenOxidationsmittel: Elektronenakzeptor („Elektronenräuber"); wird bei der Reaktion selbst reduziert. [Eselsbrücke: Putzmittel]
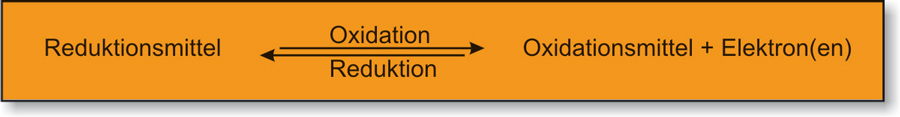
Reduktionsmittel: Elektronendonator („Elektronenspender"); wird bei der Reaktion selbst oxidiert.Redoxreaktionen: Reaktionen mit Elektronenübertragung.
Oxidation und Reduktion laufen gleichzeitig ab.Ein Reduktionsmittel gibt Elektronen ab, die es später wieder aufnehmen kann. Es wird also zu einem Oxidationsmittel.
↑ Zum Vergrößern klicken
✕
↑ Zum Vergrößern klicken
✕
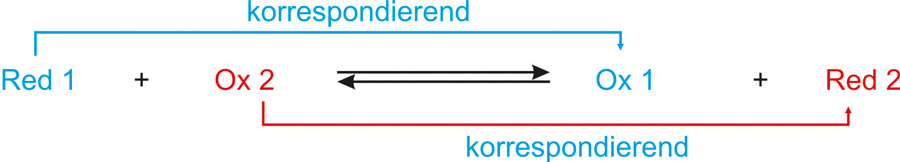
Reduktionsmittel und Oxidationsmittel bilden ein korrespondierendes Redoxpaar:
↑ Zum Vergrößern klicken
✕
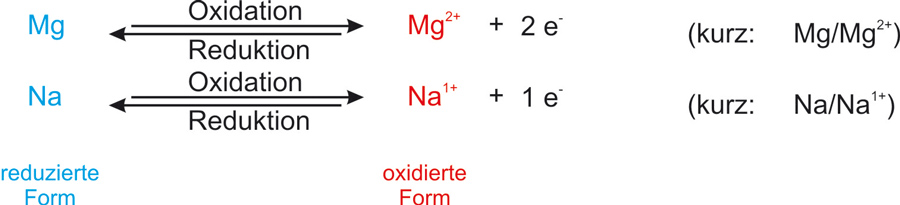
Die übliche Kurzschreibweise für ein Redoxpaar:
Reduzierte Form / oxidierte Form
Me / Men+Bei jeder Redoxreaktion sind zwei korrespondierende Redoxpaare beteiligt (analog: Protolysereaktion).
Wichtig – Elektronenbilanz
Die Zahl der abgegebenen und aufgenommenen Elektronen muss gleich sein – die Elektronenbilanz muss stimmen. Dazu multipliziert man die Teilreaktionen mit dem geeigneten gemeinsamen Vielfachen.
Auf einen Blick – die wichtigsten Aussagen
Oxidation
Oxidation = Elektronenabgabe. Die Oxidationszahl steigt. Das abgebende Teilchen heißt Reduktionsmittel und wird dabei selbst oxidiert.
Reduktion
Reduktion = Elektronenaufnahme. Die Oxidationszahl sinkt. Das aufnehmende Teilchen heißt Oxidationsmittel und wird dabei selbst reduziert.
Korrespondierendes Redoxpaar
Ox/Red-Form bilden ein Redoxpaar (Kurzschreibweise: Men+/Me). Bei jeder Redoxreaktion sind stets zwei korrespondierende Paare beteiligt.
Elektronenbilanz
Abgegebene Elektronen = aufgenommene Elektronen. Teilreaktionen mit dem gemeinsamen Vielfachen multiplizieren, bis die Bilanz stimmt.
Häufige Fragen – Freiwillig ablaufende Redoxreaktionen
Was ist der Unterschied zwischen Oxidation und Reduktion?
Oxidation ist die Abgabe von Elektronen – die Oxidationszahl des betroffenen Atoms steigt. Reduktion ist die Aufnahme von Elektronen – die Oxidationszahl sinkt. Beide Prozesse laufen immer gleichzeitig ab: Kein Teilchen gibt Elektronen ab, ohne dass ein anderes sie sofort aufnimmt. Man spricht daher von einer Redoxreaktion. Grundlagen: → Neue Definitionen Kl. 9
Was versteht man unter einem korrespondierenden Redoxpaar?
Ein korrespondierendes Redoxpaar besteht aus der oxidierten und der reduzierten Form eines Teilchens, z. B. Mg2+/Mg oder O/O2−. Kurzschreibweise: Ox-Form / Red-Form bzw. Men+/Me. Bei jeder Redoxreaktion sind genau zwei solcher Paare beteiligt – analog zu den zwei korrespondierenden Säure-Base-Paaren bei der Protolyse.
Wie unterscheiden sich Oxidationsmittel und Reduktionsmittel?
Das Oxidationsmittel ist der Elektronenakzeptor: Es nimmt Elektronen auf und wird dabei selbst reduziert (Eselsbrücke: „Putzmittel oxidiert = nimmt auf"). Das Reduktionsmittel ist der Elektronendonator: Es gibt Elektronen ab und wird dabei selbst oxidiert. Im Beispiel Mg + O₂ ist Mg das Reduktionsmittel, O₂ das Oxidationsmittel.
Wie muss die Elektronenbilanz bei einer Redoxreaktion aussehen?
Die Anzahl der abgegebenen Elektronen (Oxidation) muss exakt gleich der Anzahl der aufgenommenen Elektronen (Reduktion) sein. Um das zu erreichen, multipliziert man die Teilreaktionen mit geeigneten ganzzahligen Faktoren (kleinstes gemeinsames Vielfaches). Beispiel Mg + O₂: Die Oxidation (2 e− pro Mg) wird mit 2 multipliziert, die Reduktion (4 e− pro O₂) bleibt 1× → 4 e− auf beiden Seiten.
Was ist der Unterschied zwischen der atomaren und der molekularen Schreibweise der Reaktionsgleichung?
Die atomare Schreibweise (vereinfacht) betrachtet nur einzelne Atome und ist gut für das Verständnis der Elektronenübertragung. Die molekulare Schreibweise berücksichtigt den tatsächlichen Aggregatzustand der Stoffe (O₂ liegt molekular vor) und liefert die vollständige, ausbalancierte Reaktionsgleichung: 2 Mg + O2 → 2 MgO (ΔH < 0).
Lernkarten – Freiwillig ablaufende Redoxreaktionen
Klicke auf eine Karte, um die Antwort zu sehen.
1Was bedeutet Oxidation im Sinne der Elektronenübertragung?
Oxidation = Elektronenabgabe
→ Oxidationszahl steigt
→ Das abgebende Teilchen heißt Reduktionsmittel
(wird selbst oxidiert)2Was bedeutet Reduktion im Sinne der Elektronenübertragung?
Reduktion = Elektronenaufnahme
→ Oxidationszahl sinkt
→ Das aufnehmende Teilchen heißt Oxidationsmittel
(wird selbst reduziert)3Was versteht man unter einem korrespondierenden Redoxpaar? Gib die Kurzschreibweise an.
Ox-Form und Red-Form eines Teilchens bilden ein Paar.
Kurzschreibweise: Men+/Me
(erst oxidierte, dann reduzierte Form)
Bei jeder Redoxreaktion: 2 Paare4Woran erkennt man das Oxidationsmittel und das Reduktionsmittel in einer Reaktion?
Oxidationsmittel:
nimmt e− auf → wird reduziert
Reduktionsmittel:
gibt e− ab → wird oxidiert
Merke: Jedes Oxidationsmittel wird selbst reduziert.5Stelle die Teilreaktionen für 2 Na + Cl₂ → 2 NaCl auf und prüfe die Elektronenbilanz.
Oxidation: Na → Na+ + e− | ·2
Reduktion: Cl2 + 2 e− → 2 Cl− | ·1
————————————
2 Na + Cl2 → 2 Na+ + 2 Cl−
Bilanz: 2 e− abg. = 2 e− aufg. ✓Weiter im Kapitel Elektrochemie
← Elektrochemie – Übersicht → 1 Freiwillig ablaufende Reaktionen – Teil B → 1.2 Erstellung einer Redoxreihe
🔁 Grundlagen (Kl. 9): Magnesium + Sauerstoff · Neue Definitionen Oxidation / Reduktion · Oxidationszahlen
-
1. Magnesium und Sauerstoff
Redoxreaktionen
1. Bildung von Ionenverbindungen bei Hauptgruppenelementen
1.1 Magnesium + Sauerstoff
Experiment: Magnesiumband wird an der Luft entzündet. Es brennt mit sehr heller Flamme.
a) Vereinfacht: Alle Elemente als Atome geschrieben.
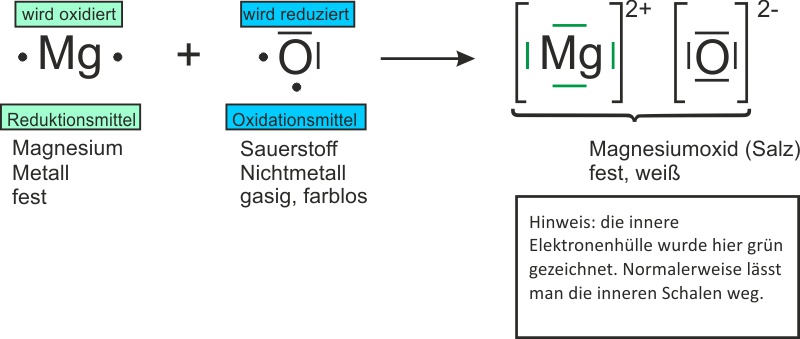
b) keine Vereinfachung: Sauerstoff wird als Molekül geschrieben:Reaktionsgleichung: 2 Mg + O2 → 2 MgO ΔH < 0
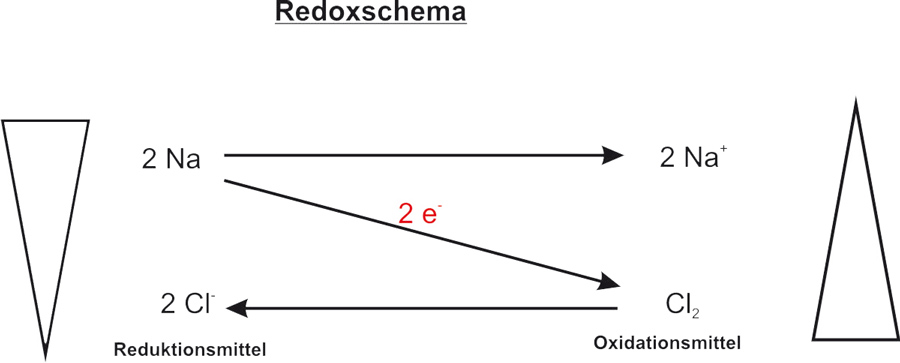
c) Redoxschema:
I. Allgemein:
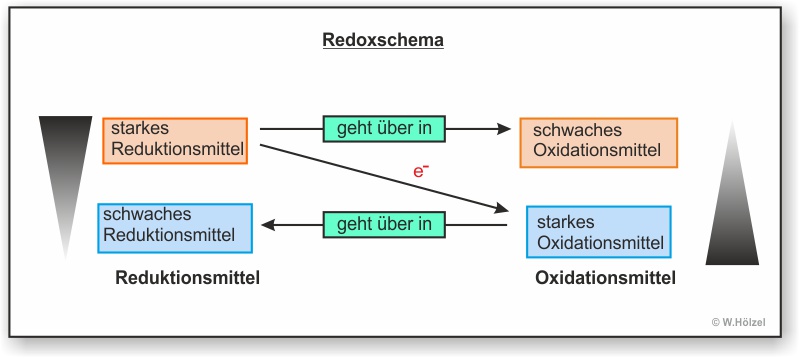
Hier erst mal das Redoxschema einer freiwillig ablaufenden Reaktion (Bergabreaktion). Mit Hilfe eines Redoxschemas kann man eine Reaktion veranschaulichen. Auf dem diagonalen Pfeil schreibt man die Anzahl der Elektronen, die von einem Stoff (bzw. Teilchen) zu einem anderen Teilchen übergehen. Oben links steht das Teilchen, welches die Elektronen abgibt. Wenn dieses Teilchen diese Elektronen abgibt verändert es sich selbst (Natrium ist zum Beispiel ein sehr reaktives Metall; Natrium-Kation hingegeben ist reaktionsarm und wir nutzen es als Bestandteil des Speisesalzs). Das oxidierte Teilchen wird oben rechts geschrieben.
Unten rechts steht das Teilchen, welches Elektronen aufnimmt. Auch dieses Teilchen verändert sich dabei. Das Ergebnis steht dann unten links.
II. Mg + O2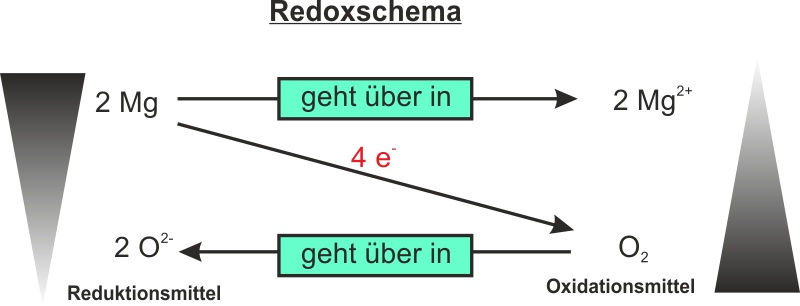
d) Teilgleichungen
Gerade bei komplizierten Redoxgleichungen, kann es eine Hilfe sein, dass man die Reaktionsgleichungen in die Teilreaktionen Oxidation und Reduktion aufsplittet. Das Ergebnis für die Verbrennung von Magnesium sind man in den folgenden Teilgleichungen. Da die Anzahl der aufgenommenen und abgegebenen Elektronen gleich sein muss, multipliziert man die Oxidationsreaktion mit zwei. Dadurch geben zwei Magnesium-Atome vier Elektronen ab (siehe Redox) und das Sauerstoffmolekül nimmt vier Elektronen auf.
Oxidation: Mg → Mg2+ + 2 e- | · 2
Reduktion: O2 + 4 e- → 2 O2- | · 1---------------------------------------------------
Redox: 2 Mg + O2 → 2 Mg2+ + 2 O2-
-
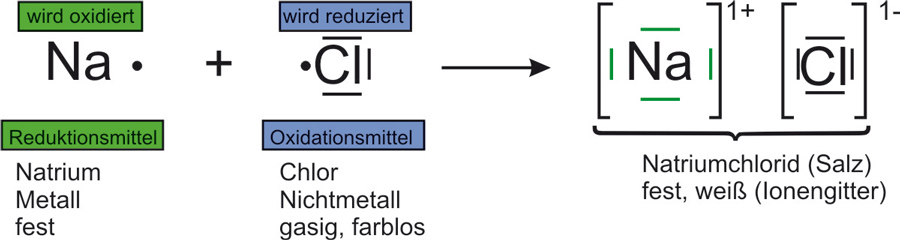
1.2 Natrium + Chlor
1.2 Natrium reagiert mit Chlor
Wichtiger Tipp: Durch Elektronenabgabe oder Aufnahme können Ionen entstehen, die Edelgaskonfigurationin der Elektronenhülle aufweisen.
- Formuliert die Teilreaktionen (Oxidation und Reduktion).
- Formuliert die Gesamtreaktion.
- Zeichnet ein vollständiges Redoxschema für diese Reaktion.
{slider title="Lösung" open="false" class="icon"}
Oxidation: Na → Na¹⁺ + 1 e⁻ | · 2
Reduktion: Cl₂ + 2 e⁻ → 2 Cl¹⁻ | · 1
-------------------------------------------
Redox: 2 Na + Cl₂ → 2 Na¹⁺ + 2 Cl¹⁻Reaktionsgleichung: 2 Na + Cl₂ → 2 NaCl ΔH < 0
{/sliders}
-
1.3 Neue Definitionen
1.3 Neue Definitionen
Oxidation= Elektronenabgabe
Reduktion= ElektronenaufnahmeRedoxreaktionen: Reaktionen mit Elektronenübertragung.
Oxidation und Reduktion laufen gleichzeitig ab.Oxidationsmittel: Elektronenakzeptor („Elektronenräuber“)
Reduktionsmittel: Elektronendonator („ Elektronenspender“) [ nicht freiwillig ]Merke: Ein Oxidationsmittel oxidiert ein anderes Teilchen und wird dabei selber reduziert.
Ein Reduktionsmittel gibt Elektronen ab, die es später wieder aufnehmen kann. Es wird also zu einem Oxidationsmittel.
Redoxpaar: z.B.
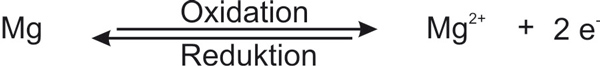
Jede Redoxreaktion man formal in zwei Teilreaktionen zerlegen:
(1) Oxidation (Elektronenabgabe)
(2) Reduktion (Elektronenaufnahme).Beispiel: Lithium reagiert mit Chlor
(1) Oxidation: Li → Li⁺ + 1 e⁻ | · 2
(2) Reduktion: Cl₂ + 2 e⁻ → 2 Cl⁻ | · 1
______________________________________________________
Teilchengleichung: 2 Li + Cl₂ → 2 Li⁺ + 2 Cl⁻
Reaktionsgleichung: 2 Li(s) + Cl₂ (g) → 2 LiCl(s) ΔH < 0Achtung:
Die Zahl der abgegebenen und aufgenommenen Elektronen muss gleich sein; die Elektronenbilanz muss stimmen (gemeinsames Vielfaches!).Aus diesem Grund muss man das Teilschema (1) mit dem Faktor 2 multiplizieren
Die Formel für das Salz LiCl besagt, dass im festen LiCl, die Lithium-Ionen und die Chlorid-Ionen im Stoffmengenverhältnis
n(Li⁺) : n(Cl-) = 1 : 1 vorhanden sind.Aufgaben:
Formuliere für folgende Reaktionen
- die Teilreaktionen.
- Stelle abschließend jeweils die Teilchengleichung und die
- Reaktionsgleichung auf.
- Achte darauf, welche Elemente molekular vorkommen und formuliere die Molekülformel auch in den Teilreaktionen.
a) Magnesium + Chlor
b) Aluminium + Sauerstoffa) Magnesium + Chlor
{slider title="Lösung" open="false" class="icon"}
(1) Oxidation: Mg → Mg²⁺ + 2 e⁻ | · 1
(2) Reduktion: Cl₂ + 2 e⁻ → 2 Cl⁻ | · 1
-----------------------------------------------------------------------------------------
Teilchengleichung: Mg + Cl₂ → Mg²⁺ + 2 Cl⁻Reaktionsgleichung: Mg + Cl₂ → MgCl₂
Die Formel für das Salz MgCl₂ besagt, dass im festen Magnesiumchlorid, die Magnesium-Ionen und die Chlorid-Ionen im Stoffmengenverhältnis n(Mg²⁺) : n(Cl-) = 1 : 2 vorhanden sind.
{/sliders}
b) Aluminium + Sauerstoff
{slider title="Lösung" open="false" class="icon"}
(1) Oxidation: Al → Al³⁺ + 3 e⁻ | · 4
(2) Reduktion: O₂ + 4 e⁻ → 2O²⁻ | · 3
---------------------------------------------------------------------------------
Teilchengleichung: 4 Al + 3 O₂ → 4 Al³⁺ + 6 O²⁻Reaktionsgleichung: 4 Al + 3 O₂ → 2 Al₂O₃
Das Ionengitter des Aluminiumoxids ist elektrisch neutral, wenn auf zwei Aluminium-Ionen (Al³⁺) drei Oxid-Ionen (O²⁻) entfallen. Das Anzahlverhältnis muss 2 : 3 lauten: (Al³⁺)₂(O²⁻)₃ oder Al₂O₃ (Verhältnisformel).
{/sliders}
Verhältnisformeln der Salze geben das Zahlenverhältnis der Ionen im Ionengitter an!
-
1.4 Aluminium reagiert mit Brom
1.4 Aluminium + Brom
- Formuliert die Teilreaktionen (Oxidation und Reduktion).
- Formuliert die Gesamtreaktion.
- Zeichnet ein vollständiges Redoxschema für diese Reaktion.
{slider title="Lösung" open="false" class="icon"}
Die Zahl der abgegebenen und aufgenommenen Elektronen muss gleich sein; die Teilchengleichung (2) muss deshalb mit dem Faktor 3 multipliziert werden.
Für die Teilchengleichung benötigt man ganze Zahlen (1,5 Brom-Moleküle gibt es nicht!). Deshalb wird die Gleichung (3) mit dem Faktor 2 multipliziert.
Teilchengleichung: 2 Al + 3 Br₂ → 2 Al³⁺ + 6 Br⁻
Reaktionsgleichung: 2 Al + 3 Br₂ → 2 AlBr₃ ΔH < 0
Redoxschema:{/sliders}
Übungen:
Formuliere für folgende Reaktionen die Teilreaktionen. Stelle abschließend jeweils die Teilchengleichung und die Reaktionsgleichung auf. Achte darauf, welche Elemente molekular vorkommen und formuliere die Molekülformel auch in den Teilreaktionen.- Magnesium + Chlor
- Aluminium + Sauerstoff
Lösungen: Um die Lösung zu sehen, muss der Bereich darunter "markiert" werden (z.B. durch Links-Klick und ziehen über den unteren Bereich mit der Maus).
a. Magnesium + Chlor
(1) Oxidation: Mg → Mg²⁺ + 2 e⁻ | · 1
(2) Reduktion: Cl₂ + 2 e⁻ → 2 Cl⁻ | · 1
-----------------------------------------------------------------------------------------
Teilchengleichung: Mg + Cl₂ → Mg²⁺ + 2 Cl⁻Reaktionsgleichung: Mg + Cl₂ → MgCl₂
Die Formel für das Salz MgCl₂ besagt, dass im festen Magnesiumchlorid, die Magnesium-Ionen und die Chlorid-Ionen im Stoffmengenverhältnis n(Mg²⁺) : n(Cl-) = 1 : 2 vorhanden sind.
b. Aluminium + Sauerstoff
(1) Oxidation: Al → Al³⁺ + 3 e⁻ | · 4
(2) Reduktion: O₂ + 4 e⁻ → 4 O²⁻ | · 3
---------------------------------------------------------------------------------
Teilchengleichung: 4 Al + 3 O₂ → 4 Al³⁺ + 6 O²⁻Reaktionsgleichung: 4 Al + 3 O₂ → 2 Al₂O₃
Das Ionengitter des Aluminiumoxids ist elektrisch neutral, wenn auf zwei Aluminium-Ionen (Al³⁺) drei Oxid-Ionen (O²⁻) entfallen. Das Anzahlverhältnis muss 2 : 3 lauten: (Al³⁺)₂(O²⁻)₃ oder Al₂O₃ (Verhältnisformel).
Wichtig: Verhältnisformeln der Salze geben das Zahlenverhältnis der Ionen im Ionengitter an.
-
2 Bildung von Ionenverbindungen mit Nebengruppenelementen
2 Bildung von Ionenverbindungen mit Nebengruppenelementen
Je nach Reaktionspartnern reagieren die folgenden Mischungen unterschiedlich heftig. Mit Hilfe weiterer solcher Reaktionen kann man eine Reihe aufstellen (Redoxschema), welche Mischungen heftiger, welche weniger heftig oder gar nicht reagieren.
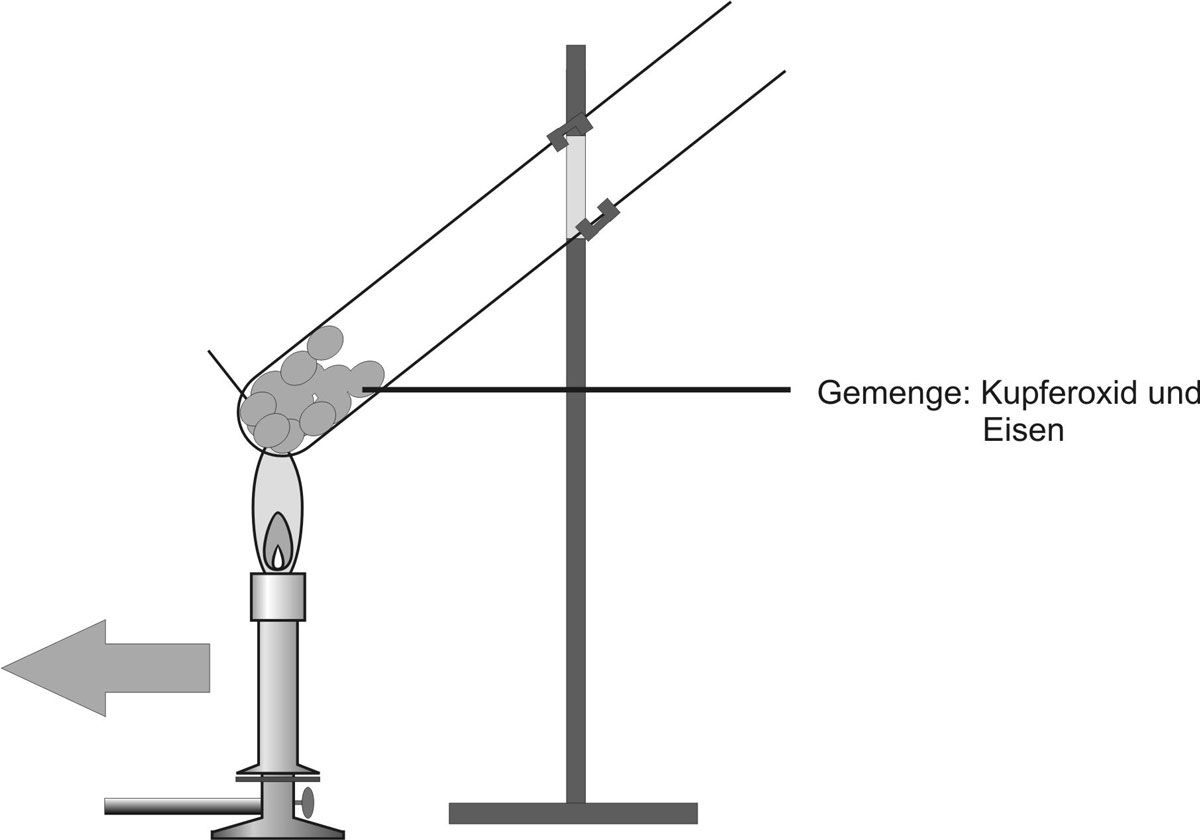
2.1 Kupferoxid + Eisen
Im Folgenden ist das Experiment dargestellt:
Teilreaktionen:
Teilchengleichung: Fe + Cu²⁺O²⁻ → Fe²⁺O²⁻ + CuRedoxschema:
Reaktionsgleichung:
Fe + CuO → FeO + Cu ΔH < 0 Eisen Kupfer(II)-oxid Eisen(II)-oxid Kupfer Metall Salz Salz Metall grau schwarz weiß rot-braun Atom Ionen Ionen Atom 2.2 Kupferoxid + Magnesium
Zum Schluss Kupferoxid ist ein Salz (Ionenverbindung) und besteht aus Cu²⁺-Ionen und O²⁻-Ionen (Oxid-Ionen)
Formuliert die Oxidation, Reduktion, Redoxreaktion, Redoxschema und Reaktionsgleichungen.
Lösung
Reduktions- und Oxidationsfähigkeit im Vergleich:
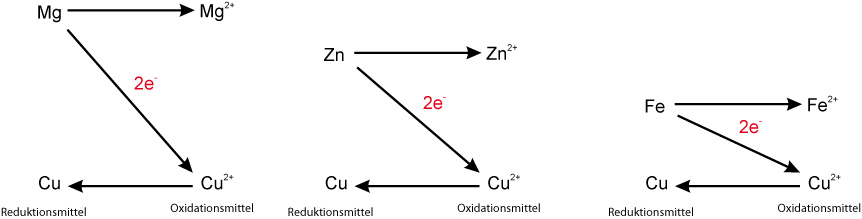
Mit Hilfe der Redoxschemata könnte man angeben, wie heftig eine Reaktion verläuft. Je größer der Abstand ist, desto stärker die Reaktion:
Eine noch praktischere Anwendung ist, sämtliche Redoxpaare in ein Diagramm zu schreiben:
Mit Hilfe dieses Diagramms kann man z.B. Voraussagen machen, ob eine Reaktion (freiwillig) abläuft oder nicht.
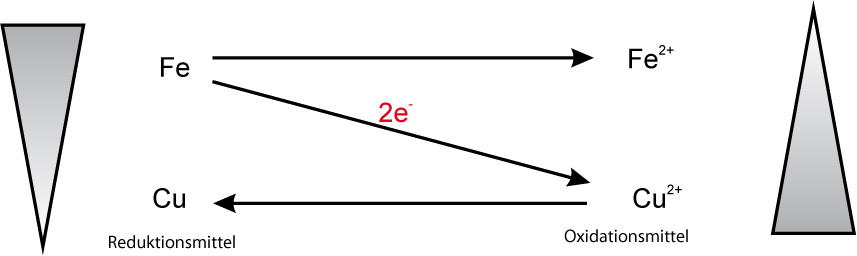
Haben wir z.B. ein Gemisch aus Eisenpulver (Fe) und Kupfer-Ionen (Cu²⁺), dann verbindet man diese beiden Teilchen im Diagramm. Da nur die linken Teilchen (Reduktionsmittel) Elektronen abgeben können, ergibt sich daraus eine "Bergab-Reaktion"; die Reaktion verläuft also freiwillig (wenn man Aktivierungsenergie zuführt).
Hätte man hingegen ein Gemisch aus Kupfer (Cu) und Eisen-Ionen (Fe²⁺), dann müssten die Kupferteilchen die Elektronen abgeben (steht ja links). Verbindet man nun diese beiden Teilchen ergibt sich eine Diagonale von links unten nach rechts oben. Hier liegt also eine "Bergauf-Reaktion" vor; der Vorgang findet nicht freiwillig statt.
Solche Diagramme sind wirklich sehr praktisch und man bekommt sie sogar zum Chemieabitur, was den Vorteil hat, dass man -sofern man die Redox-Schemata verstanden hat- relativ schnell die Lösungen einfach abschreiben kann. Diese Diagramme werden ausführlich (zusammen mit dem Elektrodenpotential) in der Oberstufe (Thema Elektrochemie) besprochen. Hier schon einmal der Link (auch zu einer solchen ausführlichen Tabelle: 2.5 Elektrochemische Spannungsreihe der Metalle und 2.5.2 Anwendung der Spannungsreihe