Qualitative Elementaranalyse
-
01.1 Methan
Was du auf dieser Seite lernst
Methan (CH₄) ist das einfachste Alkan und gleichzeitig der Einstieg in die Organische Chemie. Du lernst, wie man über die qualitative Elementaranalyse auf die Summenformel schließt, wie die Strukturformel und der Bindungswinkel aussehen, und warum die Verbrennung von Methan eine Redoxreaktion ist.
Grundlagen aus der 9. Klasse
Lewis-Formeln, Atombindung und Oxidationszahlen hast du in der 9. Klasse kennengelernt: → Lewis-Formeln (Kl. 9) · → Oxidationszahlen (Kl. 9)
1.1.1 Vorkommen
Methan kommt vor in: Erdgas, Sumpfgas, Biogas, Grubengas.
1.1.2 Eigenschaften
- farb- und geruchloses Gas
- geringere Dichte als Luft
- brennbar
1.1.3 Ermittlung der Summenformel (Molekülformel) und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
Hierfür wird der zu untersuchende Stoff verbrannt und die Verbrennungsprodukte bestimmt.
Bildet sich Wasser, ist Wasserstoff als Element vorhanden.
Kohlenstoff lässt sich als Ruß (unvollständige Verbrennung) oder als Kohlenstoffdioxid nachweisen. Der CO₂-Nachweis erfolgt mit der Kalkwasserprobe: Das entstandene Gas wird in Kalkwasser eingeleitet – eine Trübung zeigt CO₂ an.↑ Zum Vergrößern klicken
✕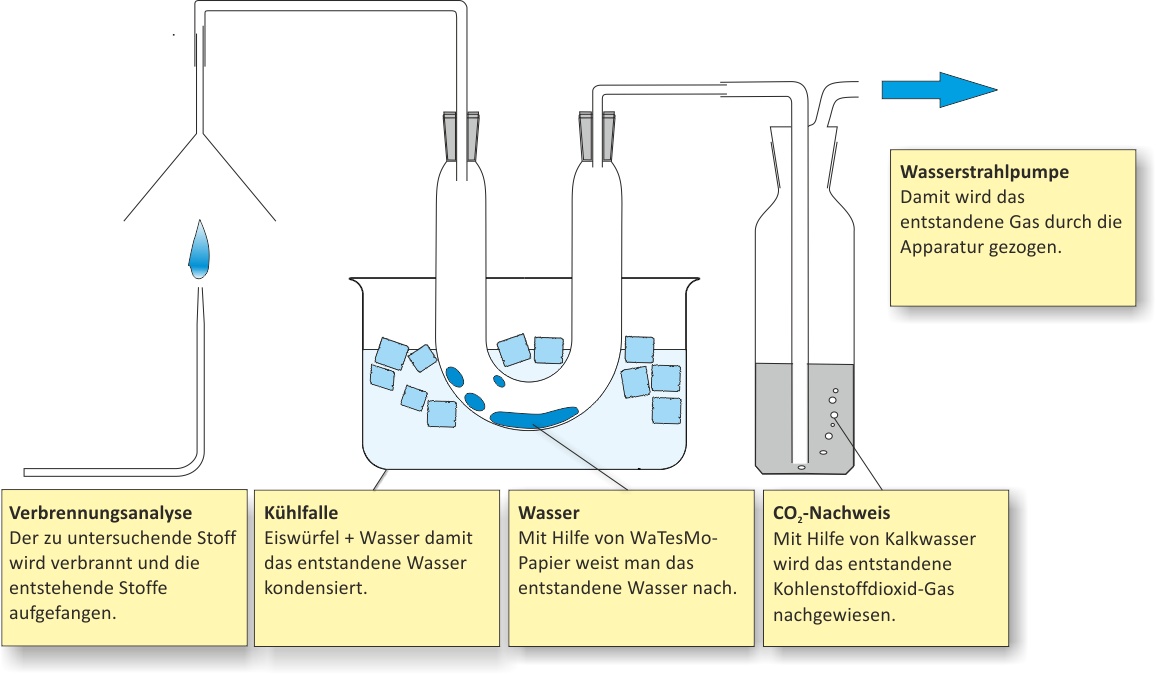
- Nachweis von Wasserstoff → Bildung von Wasser → WaTesMo-Papier oder wasserfreies Kupfersulfat.
- Nachweis von C → Bildung von CO2 → Nachweis als CaCO3:
Ca(OH)2 (aq) + CO2 (g) → CaCO3 (s) + H2O (l)
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bestimmung der molaren Masse
Mit der Gaswägung lässt sich die molare Masse von Methan bestimmen: M(Methan) = 16 g/mol · Molekülmasse 16 u.c) Summenformel: CH4
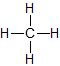
d) Strukturformel
Man zeichnet Methan meist mit einem Winkel von 90°. Dieser Winkel entspricht nicht dem tatsächlichen Bindungswinkel (vgl. unten). Man kann sich aber vorstellen, dass man direkt auf das Molekül blickt.↑ Zum Vergrößern klicken
✕ ✕
✕
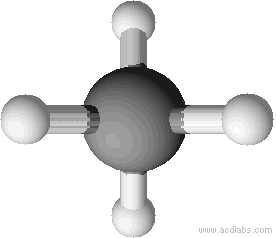
Tetraedrische Anordnung der Wasserstoffatome um das Kohlenstoffatom (Bindungswinkel 109,5°). Erklärung: größtmögliche Entfernung der Wasserstoffatome.
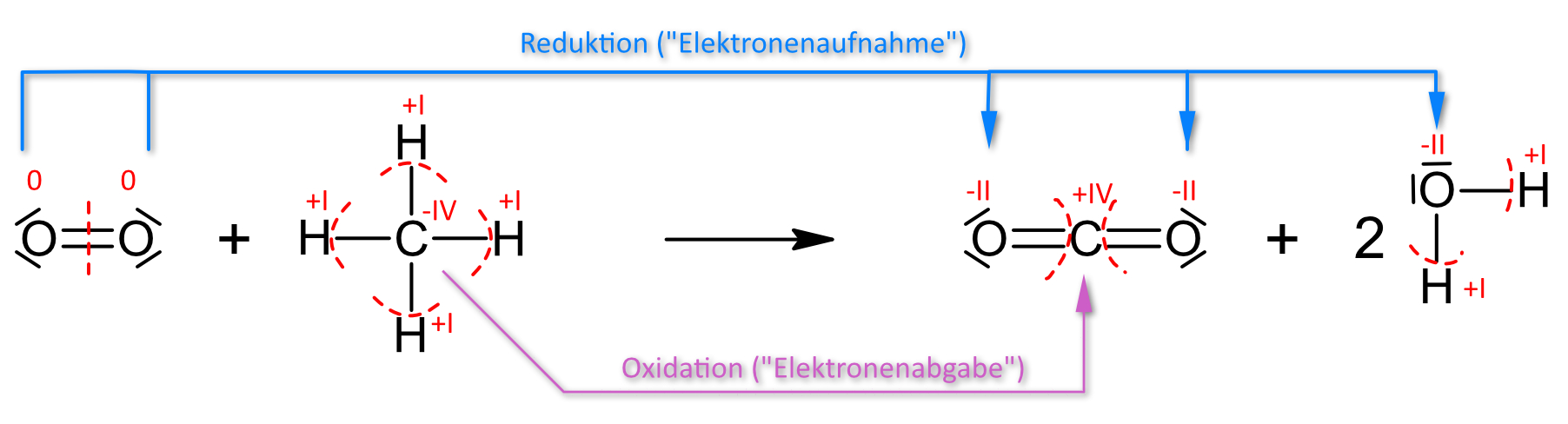
1.1.4 Vollständige Verbrennung
0 −IV +I +IV −II +I −II
2 O2 + CH4 → CO2 + 2 H2O ΔH = −888 kJ/mol↑ Zum Vergrößern klicken
✕
Hinweis: Wenn die Ermittlung der Oxidationszahlen Schwierigkeiten macht, kann man es hier nochmals nachlesen.
1 l Methan benötigt zur vollständigen Verbrennung 10 Liter Luft (2 l Sauerstoff).
Auf einen Blick – Methan
Summenformel
Methan: CH₄ · molare Masse 16 g/mol · einfachstes Alkan · allg. Formel der Alkane: CₙH₂ₙ₊₂ (hier n = 1).
Tetraeder
Die vier H-Atome ordnen sich tetraedrisch um das C-Atom an. Bindungswinkel: 109,5° (größtmögliche Abstoßung der Bindungselektronenpaare).
Elementaranalyse
Verbrennung → H₂O (Wassernachweis: WaTesMo) + CO₂ (Kalkwasserprobe: Trübung durch CaCO₃) → Methan enthält C und H.
Verbrennung
CH₄ + 2 O₂ → CO₂ + 2 H₂O · ΔH = −888 kJ/mol (exotherm). C wird von −IV auf +IV oxidiert; O von 0 auf −II reduziert.
Häufige Fragen – Methan
Wie weist man experimentell nach, dass Methan Kohlenstoff und Wasserstoff enthält?
Methan wird vollständig verbrannt. Die entstehenden Gase und Dämpfe werden durch zwei Nachweisreagenzien geleitet: Wassernachweis mit wasserfreiem Kupfersulfat (wird blau) oder WaTesMo-Papier (Blaufärbung zeigt Wasser an) → Methan enthält Wasserstoff. CO₂-Nachweis mit Kalkwasser Ca(OH)₂: Trübung durch CaCO₃-Bildung → Methan enthält Kohlenstoff.
Warum ist der Bindungswinkel in Methan 109,5° und nicht 90°?
Die vier bindenden Elektronenpaare stoßen sich gemäß dem VSEPR-Modell (Valence Shell Electron Pair Repulsion) so weit wie möglich ab. Maximale Abstoßung ergibt eine tetraedrische Anordnung mit einem Bindungswinkel von 109,5°. In der vereinfachten Strukturformel zeichnet man 90°-Winkel, weil man so tut, als würde man von oben auf das Molekül blicken.
Warum ist die Verbrennung von Methan eine Redoxreaktion?
Bei der Verbrennung ändert sich die Oxidationszahl des Kohlenstoffs von −IV (in CH₄) auf +IV (in CO₂) → Oxidation. Der Sauerstoff wird von 0 (O₂) auf −II (in CO₂ und H₂O) reduziert → Reduktion. Es findet also ein Elektronenübergang statt: Methan ist das Reduktionsmittel, Sauerstoff das Oxidationsmittel. → Oxidationszahlen (Kl. 9)
Was bedeutet ΔH = −888 kJ/mol bei der Verbrennung?
Das negative Vorzeichen zeigt, dass Energie abgegeben wird – die Reaktion ist exotherm. Pro Mol verbranntem Methan (= 16 g) werden 888 kJ Wärmeenergie freigesetzt. Das erklärt, warum Methan (Erdgas) als Energieträger zum Heizen und Kochen eingesetzt wird. Mehr zur Reaktionsenthalpie: → Enthalpie (Kursstufe)
Wo kommt Methan natürlich vor und warum ist es klimarelevant?
Methan kommt natürlich in Erdgas (Hauptbestandteil), Sumpfgas (Zersetzung organischer Stoffe unter Wasser), Biogas (Gärung) und Grubengas (Steinkohlebergbau) vor. Als Treibhausgas ist CH₄ etwa 25-mal klimawirksamer als CO₂ (bezogen auf 100 Jahre), weil es Infrarotstrahlung besonders effektiv absorbiert.
Lernkarten – Methan
Klicke auf eine Karte, um die Antwort zu sehen.
1Gib Summenformel, molare Masse und Bindungswinkel von Methan an.
Summenformel: CH₄
Molare Masse: 16 g/mol
Bindungswinkel: 109,5° (Tetraeder)
Struktur: 4 H-Atome tetraedrisch um C2Wie weist man bei der Elementaranalyse Kohlenstoff und Wasserstoff nach?
H-Nachweis:
WaTesMo-Papier oder CuSO₄ (wasserfrei) → Blaufärbung = H₂O vorhanden
C-Nachweis:
Kalkwasser Ca(OH)₂ → Trübung = CO₂ vorhanden3Stelle die vollständige Verbrennungsgleichung von Methan auf.
CH₄ + 2 O₂ → CO₂ + 2 H₂O
ΔH = −888 kJ/mol (exotherm)
Kontrolle: C: 1=1 ✓ · H: 4=4 ✓ · O: 4=4 ✓4Welche Oxidationszahlen hat Kohlenstoff in CH₄ und in CO₂? Was folgt daraus?
CH₄: C hat Oxidationszahl −IV
CO₂: C hat Oxidationszahl +IV
→ Oxidationszahl steigt → C wird oxidiert
→ Methan = Reduktionsmittel5Wieviel Liter Luft benötigt 1 l Methan zur vollständigen Verbrennung, und warum?
10 Liter Luft (≈ 2 l O₂, da Luft ≈ 21 % O₂)
CH₄ + 2 O₂ → … · Stöchiometrie: 1 Vol. CH₄ : 2 Vol. O₂
Luft enthält ~20 % O₂ → 2 l O₂ stecken in 10 l LuftWeiter im Kapitel Alkane
← 1 Alkane – Übersicht → 1.4 Butan → 1.5 Homologe Reihe
🔁 Grundlagen (Kl. 9): Lewis-Formeln · Oxidationszahlen
📚 Vertiefung Kursstufe: Enthalpie ΔH -
01.4 Butan
Was du auf dieser Seite lernst
Butan (C₄H₁₀) ist das erste Alkan, das in zwei verschiedenen Strukturen vorkommt. Du lernst den zentralen Begriff der Konstitutionsisomerie kennen, verstehst warum n-Butan und Isobutan verschiedene Siedepunkte haben, und übst die Halbstrukturformel als platzsparende Schreibweise.
Grundlagen aus 1.1 Methan
Summenformel, Strukturformel und Lewis-Formel hast du am Beispiel Methan kennengelernt: → 1.1 Methan · → Lewis-Formeln (Kl. 9)
Hinweis: 1.2 Ethan und 1.3 Propan werden nur bei ausreichend Zeit besprochen. Da sie ähnlich aufgebaut sind, wird auf einen eigenen Heftaufschrieb verzichtet (vgl. 1.5 Homologe Reihe).
1.4.1 Vorkommen
Im Erdgas; fällt an bei der Benzingewinnung.
1.4.2 Eigenschaften
Farbloses Gas · größere Dichte als Luft · brennbar (Verbrennungsprodukte bei vollständiger Verbrennung: CO2 und H2O) · unter Druck leicht verflüssigbar.
1.4.3 Ermittlung der Summenformel und Strukturformel
a) Qualitative Analyse (Elementaranalyse)
↑ Zum Vergrößern klicken
✕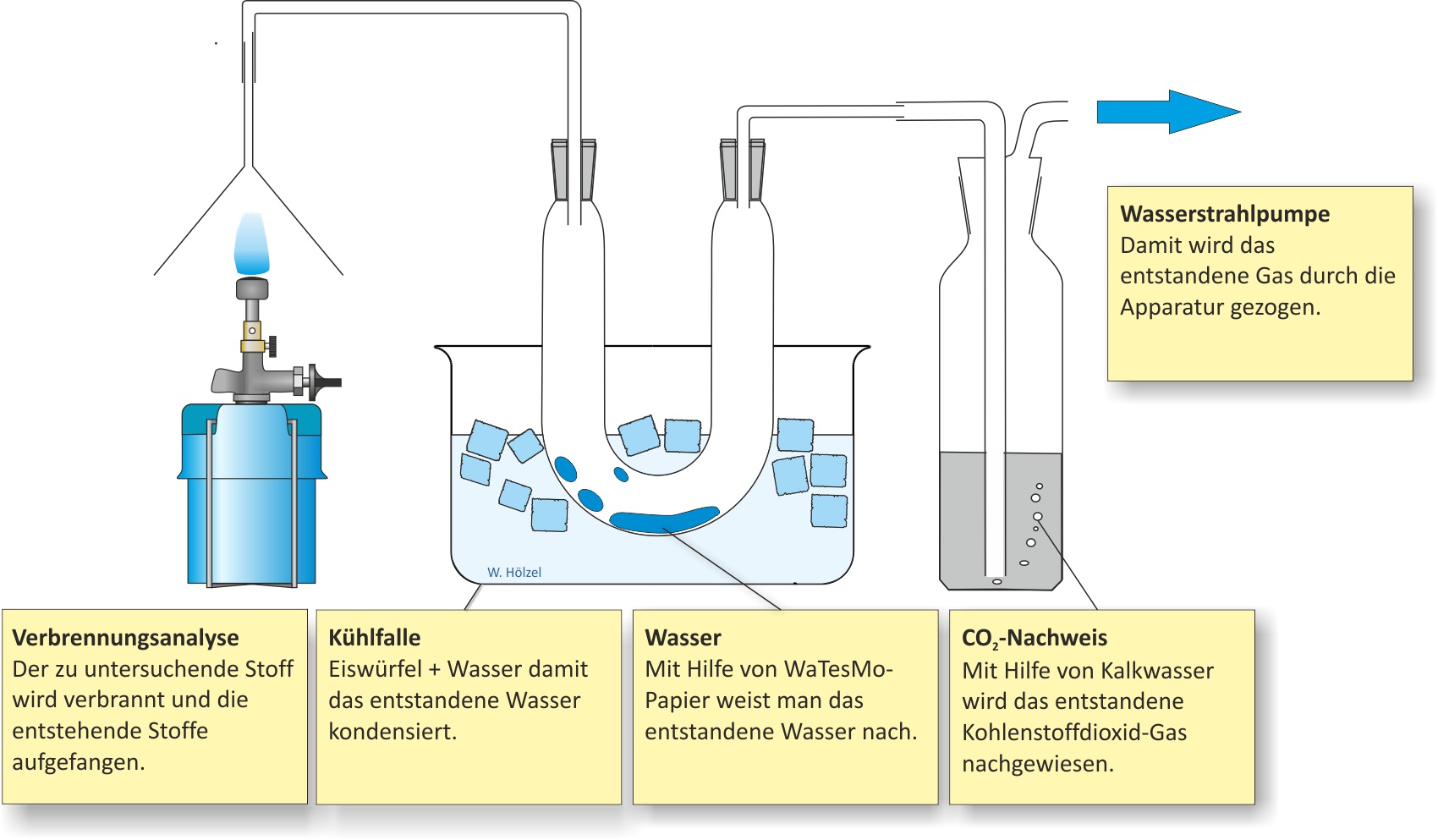
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) zeigen, dass Butan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält.
b) Bau und Formeln
1. Molare Masse = 58,12 g/mol · Molekülmasse = 58,12 u
2. Summenformel: C4H103. Strukturformel – zwei Möglichkeiten:
✕ ✕
✕
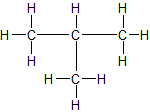
ZMK: nur Van-der-Waals-Kräfte. Bei n-Butan können sich die Moleküle dichter zusammenlagern → stärkere ZMK → etwas höhere Siedetemperatur als Isobutan.
Räumliche Strukturen im Kugelstabmodell (versuche, die Abbildungen n-Butan oder Isobutan zuzuordnen):
✕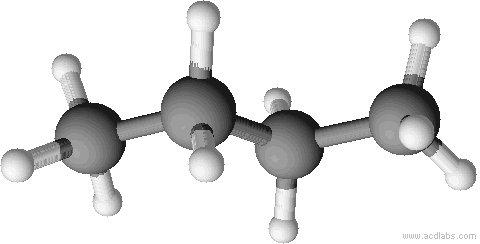 ✕
✕
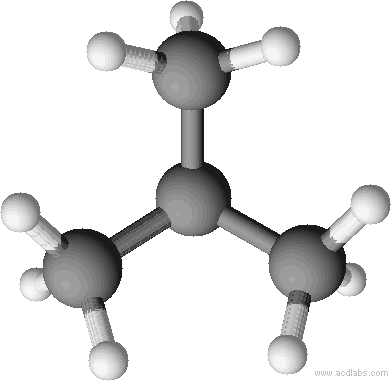
Renderbild n-Butan als Kugelstabmodell:
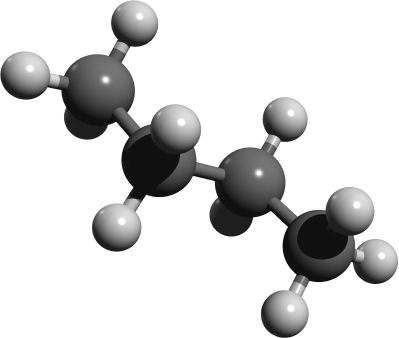
Kalottenmodell von 2-Methylpropan (= Isobutan) – bei Kalottenmodellen wird die Raumfüllung der Atome sichtbar:
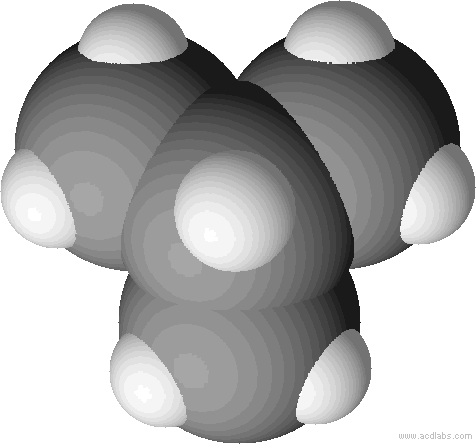
Da Strukturformeln bei größeren Molekülen zu aufwendig sind, nutzt man die Halbstrukturformel: Die Wasserstoffatome werden als Summe direkt hinter das jeweilige C-Atom geschrieben. Man ermittelt zunächst, wie viele Bindungen ein C-Atom bereits hat, und ergänzt H-Atome bis zur Vierbindigkeit. Hier am Beispiel Isobutan:
↑ Zum Vergrößern klicken
✕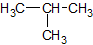
1.4.4 Verwendung
Heizgas („blaue Gaskartuschen") · Kältemittel (Ersatz für FCKW) · Treibgas in Sprays · Feuerzeuggas (häufig zusammen mit Propan).
1.4.5 Isomerie
(isos (griech.) = gleich; meros (griech.) = Teil)
Definition – Konstitutionsisomerie
Verbindungen, deren Moleküle bei gleicher Summenformel unterschiedliche Strukturformeln besitzen, bezeichnet man als Isomere. Isomere unterscheiden sich vor allem in ihren physikalischen Eigenschaften (Schmelz- und Siedepunkt) und wenig in ihren chemischen Reaktionen.
1.4.6 Vollständige Verbrennung (Oxidation)
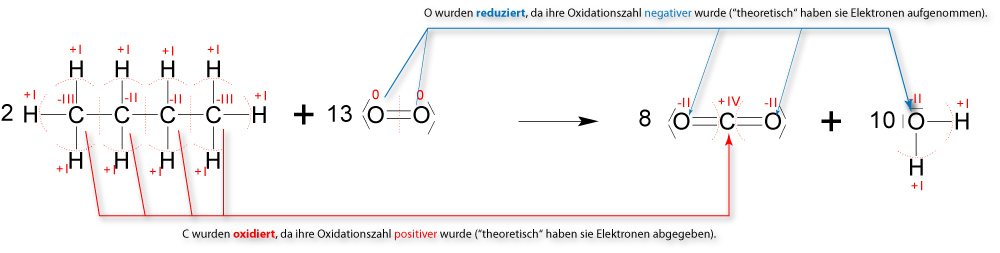
Wenn Butan vollständig verbrannt wird, entstehen ausschließlich Kohlenstoffdioxid und Wasser:
↑ Zum Vergrößern klicken
✕
Auf einen Blick – Butan
Summenformel
C4H10 · molare Masse 58,12 g/mol · stimmt mit der allg. Formel CₙH₂ₙ₊₂ überein (n = 4 → 4·2+2 = 10 H).
Konstitutionsisomerie
n-Butan (Sdp. −0,5 °C) und Isobutan = 2-Methylpropan (Sdp. −12 °C) haben die gleiche Summenformel C₄H₁₀, aber verschiedene Strukturformeln.
ZMK und Siedepunkt
Nur Van-der-Waals-Kräfte. n-Butan lagert sich dichter zusammen → stärkere ZMK → höherer Siedepunkt als das verzweigte Isobutan.
Halbstrukturformel
H-Atome als Summe hinter das C schreiben. n-Butan: CH₃–CH₂–CH₂–CH₃ · Isobutan: CH₃–CH(CH₃)–CH₃ · Vierbindigkeit von C muss stets erfüllt sein.
Häufige Fragen – Butan
Was versteht man unter Konstitutionsisomerie?
Konstitutionsisomere sind Verbindungen mit gleicher Summenformel, aber unterschiedlicher Verknüpfung der Atome. Bei C₄H₁₀ gibt es zwei Isomere: n-Butan (unverzweigte Kette) und 2-Methylpropan (Isobutan) (verzweigte Kette). Sie unterscheiden sich in physikalischen Eigenschaften wie dem Siedepunkt, kaum aber in chemischen Reaktionen. Mit steigender C-Zahl nimmt die Zahl möglicher Isomere stark zu (C₅: 3, C₁₀: 75).
Warum hat n-Butan einen höheren Siedepunkt als Isobutan?
Beide Isomere sind unpolar und besitzen nur Van-der-Waals-Kräfte als Wechselwirkung zwischen den Molekülen. Die gestreckte Kette von n-Butan ermöglicht eine größere Kontaktfläche zwischen benachbarten Molekülen als die kompaktere, kugelförmigere Gestalt von Isobutan. Größere Kontaktfläche → stärkere Van-der-Waals-Kräfte → höherer Siedepunkt (n-Butan: −0,5 °C; Isobutan: −12 °C).
Was ist der Unterschied zwischen Strukturformel, Halbstrukturformel und Summenformel?
Die Summenformel gibt nur die Anzahl der Atome an (C₄H₁₀), nicht deren Anordnung. Die Strukturformel zeigt alle Bindungsstriche explizit – anschaulich, aber bei großen Molekülen aufwendig. Die Halbstrukturformel ist ein Kompromiss: Das C-Gerüst wird ausgeschrieben, H-Atome werden als Anzahl hinter das jeweilige C-Atom gesetzt. Isobutan: CH₃–CH(CH₃)–CH₃ · n-Butan: CH₃–CH₂–CH₂–CH₃.
Wofür wird Butan im Alltag verwendet?
Butan wird wegen seiner leichten Verflüssigbarkeit unter Druck vielfältig eingesetzt: als Heizgas in Gaskartuschen beim Camping, als Kältemittel (FCKW-Ersatz in Kühlschränken), als Treibgas in Sprühdosen und als Feuerzeuggas (oft zusammen mit Propan).
Wie lautet die ausgeglichene Verbrennungsgleichung für n-Butan?
Vollständige Verbrennung:
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle: C: 8 = 8 ✓ · H: 20 = 20 ✓ · O: 26 = 26 ✓
Die Reaktion ist stark exotherm – deshalb wird Butan als Brennstoff genutzt.Lernkarten – Butan
Klicke auf eine Karte, um die Antwort zu sehen.
1Gib Summenformel und molare Masse von Butan an. Prüfe die allg. Alkan-Formel.
Summenformel: C₄H₁₀
Molare Masse: 58,12 g/mol
Formel CₙH₂ₙ₊₂ mit n=4: 2·4+2 = 10 H ✓2Was sind Konstitutionsisomere? Nenne die beiden C₄H₁₀-Isomere mit Siedepunkten.
Gleiche Summenformel, verschiedene Struktur:
n-Butan: unverzweigt · Sdp. −0,5 °C
2-Methylpropan (Isobutan): verzweigt · Sdp. −12 °C3Schreibe n-Butan und Isobutan als Halbstrukturformel.
n-Butan:
CH₃–CH₂–CH₂–CH₃
Isobutan (2-Methylpropan):
CH₃–CH(CH₃)–CH₃4Warum hat n-Butan einen höheren Siedepunkt als Isobutan, obwohl beide C₄H₁₀ sind?
Nur Van-der-Waals-Kräfte vorhanden.
n-Butan: gestreckte Kette → größere Kontaktfläche
→ stärkere VdW-Kräfte → höherer Siedepunkt
Isobutan: kompaktere Form → weniger Kontakt5Stelle die ausgeglichene Verbrennungsgleichung für n-Butan auf.
2 C₄H₁₀ + 13 O₂ → 8 CO₂ + 10 H₂O
Kontrolle:
C: 2·4 = 8 | 8·1 = 8 ✓
H: 2·10 = 20 | 10·2 = 20 ✓
O: 13·2 = 26 | 8·2+10 = 26 ✓Weiter im Kapitel Alkane
← 1.1 Methan → 1.5 Homologe Reihe → 1.6 Nomenklatur
🔁 Grundlagen: 1.1 Methan · Lewis-Formeln (Kl. 9)
📚 Vertiefung: Isomerie bei Alkenen · Isomerie (Kursstufe) -
3.1 Ethin (Acetylen)
3.1 Ethin (Acetylen)
3.1.1 Eigenschaften
a) physikalische Eigenschaften
- farbloses Gas (geruchslos)
- leichter als Luft
- Smp.: -80,8°C
- Sdp.: - 84°C (Sublimation)
b) chemische
- brennt mit stark leuchtender und rußender Flamme
- entfärbt Bromwasser
- bildet mit Luft ein explosives Gemisch
- zerfällt unter Druck explosionsartig (⇨ nicht in Druckflaschen)
3.1.2 FormelermittlungVerbrennungsprodukte: H₂O, CO₂ (und bei unvollständiger Verbrennung C)
Molare Masse: M(Ethin) = 26 g/mol
Ermittel aus der molaren Masse die Summen- und die Strukturformel:
{slider title="Lösung" open="false" class="icon"}
Summenformel: C₂H₂
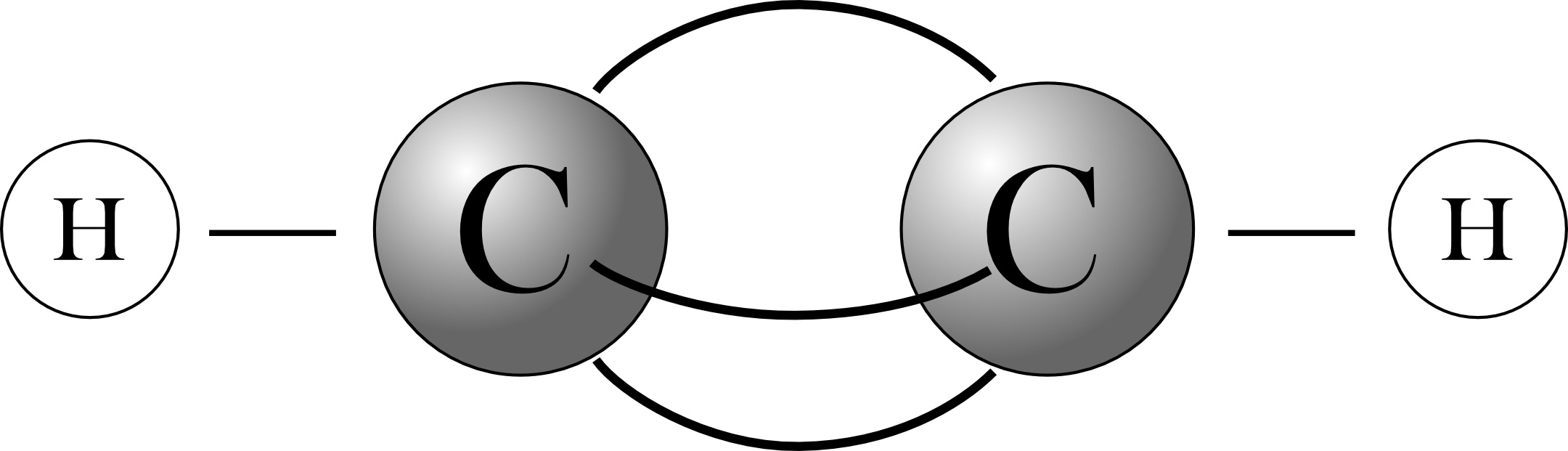
Strukturformel:
(linear; Bindungswinkel 180°)Bindungslänge noch geringer als bei der Doppelbindung (C=C: 134 pm; C=-C: 120 pm)
Ballmodell:3 „Bananenbindungen“, alle 4 Atome sind linear angeordnet.
{/sliders}
-
5 Alkohole - Alkanole
Was du in diesem Kapitel lernst
Alkohole (Alkanole) sind Kohlenwasserstoffe mit mindestens einer OH-Gruppe (Hydroxygruppe). Am Beispiel des Ethanols lernst du Eigenschaften, Formelermittlung und typische Reaktionen kennen. Dazu kommen die homologe Reihe, der induktive Effekt und die wichtigen mehrwertigen Alkohole wie Glycerin und Glykol.
Grundlagen aus der 10. Klasse
Alkohole enthalten eine C-Kette wie die Alkane, Alkene und Alkine. Wiederhole bei Bedarf: → 3. Alkine – C≡C-Dreifachbindung, Additionsreaktion · → 2. Alkene – Funktionelle Gruppen, Isomerie
Kapitelübersicht – 5. Alkohole (Alkanole)
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
5.1 Ethanol
C₂H₅OH5.1
Ethanol
Herstellung · Physikalische & chemische Eigenschaften · Alkoholismus
→ 5.1.1 Herstellung · 5.1.2 Eigenschaften · 5.1.6 Alkoholismus5.1.3
Formelermittlung
Verbrennungsanalyse · Summen- und Strukturformel von Ethanol · Molare Masse
5.1.4
Ethanol + Alkalimetall
Versuch: Natrium in Ethanol · Reaktionsgleichung · Vergleich mit Wasser
5.1.5
Induktiver Effekt
+I-Effekt und −I-Effekt · Elektronenverschiebung · Polarität der O–H-Bindung
5.2 Homologe Reihe & Systematik
5.2
Homologe Reihe der Alkohole
Hydroxy- & Methylgruppe · wichtige Alkohole · Löslichkeit · H-Brückenbindung
→ 5.2.1 Gruppen · 5.2.2 Wichtige Alkohole · 5.2.3 Löslichkeit5.2.4 / 5.2.5
Primär · Sekundär · Tertiär
Unterscheidung nach C-Nachbarn · allgemeine Formel der Alkanole CnH2n+1OH
5.2.6
Mehrwertige Alkohole
Glykol (Ethandiol) · Glycerin (Propantriol) · Sorbit · Vorkommen & Verwendung
5.3 Reaktionen · 5.4 Ether
5.3
Chemische Reaktionen
Bindungsverhältnisse · Redox mit Na · Verbrennung · Reaktion mit HBr · Dehydratisierung
→ 5.3.1–5.3.5 am Beispiel von Ethanol5.4
Ether
Herstellung · Physikalische Eigenschaften · Chemische Eigenschaften · Verwendung
⚠️ Seite noch nicht online
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkohole besitzen eine oder mehrere OH-Gruppen (Hydroxygruppen). Die Formel einwertiger Alkanole lautet CnH2n+1OH. Die OH-Gruppe bestimmt die typischen Eigenschaften: Löslichkeit in Wasser, H-Brückenbindungen, Reaktivität.
Induktiver Effekt
Der negative induktive Effekt (−I) des Sauerstoffs zieht Elektronen aus der C–O-Bindung, wodurch das H in der OH-Gruppe leicht abspaltbar (schwach sauer) wird. Alkylgruppen zeigen den +I-Effekt.
prim / sek / tert
Primäre Alkohole: OH am C-Atom mit 1 C-Nachbarn. Sekundäre: 2 C-Nachbarn. Tertiäre: 3 C-Nachbarn. Die Klassifizierung bestimmt das Reaktionsverhalten (z. B. Oxidierbarkeit).
Reaktionen
Ethanol reagiert als schwache Säure mit Natrium (→ Natriumethanolat + H2), verbrennt zu CO2 + H2O und reagiert mit HBr durch nucleophile Substitution zu Bromoethan.
Häufige Fragen – Alkohole (Alkanole)
Was sind Alkohole, und was ist ihre funktionelle Gruppe?
Alkohole (Alkanole) sind organische Verbindungen mit mindestens einer Hydroxygruppe (–OH). Das einfachste Mitglied ist Methanol (CH3OH), das wichtigste im Alltag ist Ethanol (C2H5OH). Die allgemeine Formel einwertiger Alkanole lautet CnH2n+1OH. Die OH-Gruppe verleiht Alkoholen ihre charakteristischen Eigenschaften: gute Wasserlöslichkeit (durch H-Brücken), höhere Siedepunkte als vergleichbare Alkane, und schwach saures Verhalten gegenüber Alkalimetallen.
Was unterscheidet primäre, sekundäre und tertiäre Alkohole?
Die Klassifizierung richtet sich danach, an wie vielen C-Atomen das OH-tragende Kohlenstoffatom gebunden ist: Primärer Alkohol: das OH-C hat einen C-Nachbarn (z. B. Ethanol, 1-Propanol). Sekundärer Alkohol: das OH-C hat zwei C-Nachbarn (z. B. 2-Propanol = Isopropanol). Tertiärer Alkohol: das OH-C hat drei C-Nachbarn (z. B. 2-Methyl-2-propanol). Diese Unterscheidung ist entscheidend für die Oxidierbarkeit: primäre → Aldehyde → Carbonsäuren; sekundäre → Ketone; tertiäre können nicht oxidiert werden. → 5.2.4
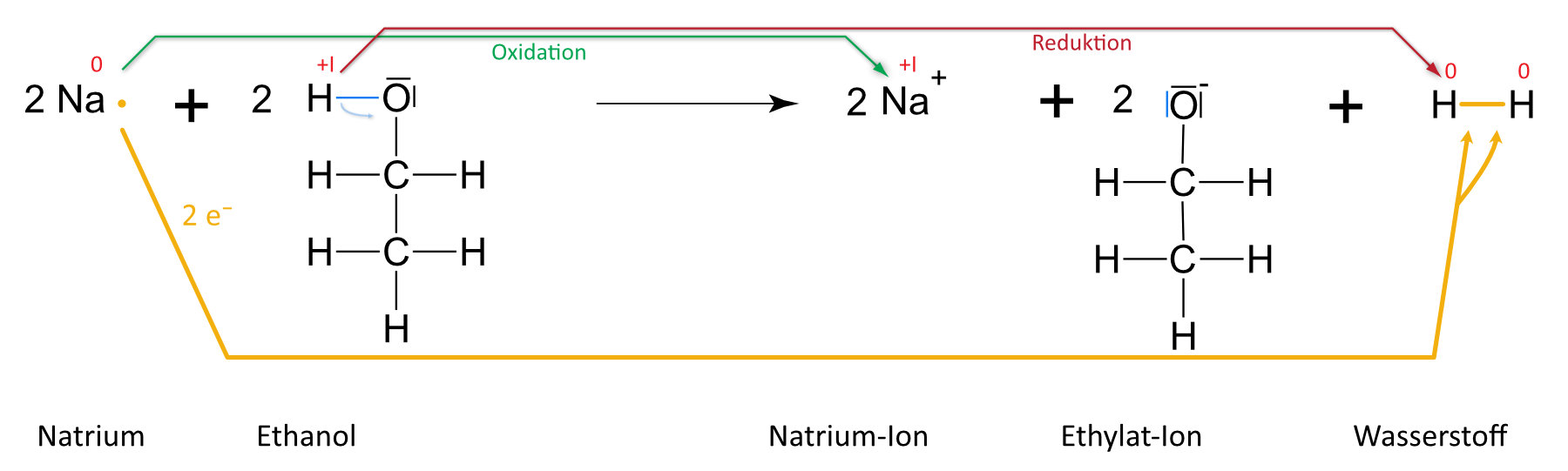
Wie reagiert Ethanol mit Natrium, und was beweist das über die OH-Gruppe?
Ethanol reagiert mit Natrium ähnlich wie Wasser, jedoch langsamer: 2 C2H5OH + 2 Na → 2 C2H5ONa + H2↑. Es entsteht Natriumethanolat und Wasserstoffgas. Die Reaktion zeigt, dass die OH-Gruppe in Alkoholen schwach sauer ist: das H-Atom der OH-Gruppe wird als H⁺ abgegeben (schwächere Säure als Wasser, weil der +I-Effekt der Ethylgruppe die O–H-Bindung weniger polarisiert). → 5.1.4
Was ist der induktive Effekt, und wie wirkt er in der OH-Gruppe?
Als induktiven Effekt bezeichnet man die Verschiebung der Elektronendichte in einer Bindungskette durch einen elektronegativen oder elektropositiven Substituenten. Der Sauerstoff der OH-Gruppe ist stark elektronegativ und zieht Elektronen aus dem benachbarten C-Atom heraus → negativer induktiver Effekt (−I). Die O–H-Bindung ist stark polarisiert, das H-Atom leicht abspaltbar. Alkylgruppen geben Elektronen ab (+I-Effekt), was die Säurestärke der Alkohole gegenüber Wasser leicht herabsetzt. → 5.1.5
Was sind mehrwertige Alkohole, und wo kommen sie vor?
Mehrwertige Alkohole tragen mehr als eine OH-Gruppe. Wichtige Vertreter: Glykol (Ethan-1,2-diol, 2 OH-Gruppen) – Frostschutzmittel und Ausgangsstoff für Kunststoffe (PET). Glycerin (Propan-1,2,3-triol, 3 OH-Gruppen) – natürlicher Bestandteil von Fetten und Ölen, Zusatz in Kosmetik, Lebensmitteln und Arzneimitteln. Sorbit (Hexan-1,2,3,4,5,6-hexol) – Zuckerersatzstoff. Durch die vielen OH-Gruppen bilden mehrwertige Alkohole besonders viele H-Brücken → sehr hohe Siedepunkte, sirupartige Konsistenz. → 5.2.6
Lernkarten – Alkohole
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkohole? Wie lautet die allgemeine Formel?
Funktionelle Gruppe: –OH (Hydroxygruppe)
Allgemeine Formel einwertiger Alkanole: CnH2n+1OH
Beispiele: Methanol CH3OH · Ethanol C2H5OH2Was ist ein primärer, sekundärer und tertiärer Alkohol? Nenne je ein Beispiel.
Primär: OH-C hat 1 C-Nachbarn → Ethanol
Sekundär: 2 C-Nachbarn → 2-Propanol
Tertiär: 3 C-Nachbarn → 2-Methyl-2-propanol
Tertiäre Alkohole sind nicht oxidierbar.3Was passiert, wenn Ethanol mit Natrium reagiert? Gleichung?
2 C2H5OH + 2 Na →
2 C2H5ONa + H2↑
Natriumethanolat + Wasserstoff. Langsamer als Na + H₂O (schwächere Säure).4Was ist Glycerin? Nenne Formel, Anzahl der OH-Gruppen und eine Verwendung.
Propan-1,2,3-triol
Formel: C3H5(OH)3
3 OH-Gruppen → sirupartig, hygroskopisch
Verwendung: Kosmetik, Lebensmittel (E422), Fettbaustein5Berechne: Wie viel g H2 entstehen bei der Reaktion von 46 g Ethanol mit überschüssigem Natrium?
2 C2H5OH + 2 Na → 2 C2H5ONa + H2
M(C2H5OH) = 46 g/mol → n = 1 mol
Verhältnis 2:1 → n(H2) = 0,5 mol
m(H2) = 0,5 · 2 g/mol = 1 g H2
Weiter im Fach Chemie / 10. Klasse
← 3. Alkine → 6. Carbonylverbindungen ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Naturstoffe – Aminosäuren, Glucose, Enzyme
-
5.1.4 Versuch Ethanol reagiert mit Alkalimetall
5.1.4 Versuch: Ethanol + Alkalimetall
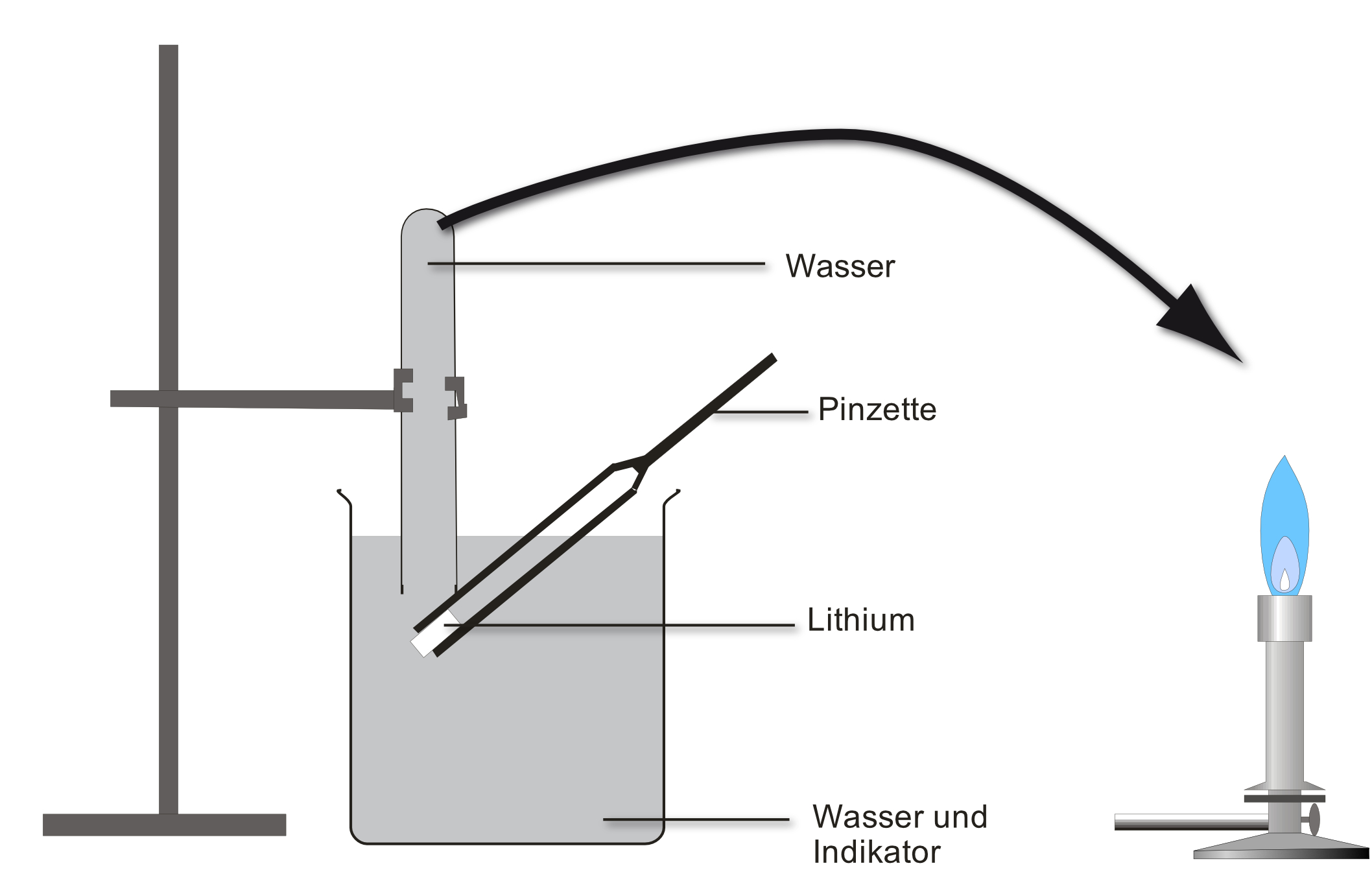
Versuch: Ein Stück Lithium ( SE ) wird auf Ethanol, Benzin und Wasser gegeben. Alternativ kann man die Experimente auch mit Natrium als Lehrerversuch durchführen. Die Reaktionsgleichungen sind mit dem Alkalimetall Natrium formuliert. Für Lithium gilt es analog.
Bei Wasser ist der Aufbau etwas komplizierter:
Beobachtung: Gasentwicklung; das entstehende Gas ist brennbar; Natrium „verschwindet“; die neu entstandene Lösung leitet den elektrischen Strom; dampft man die Lösung ein, entsteht ein weißer Feststoff.
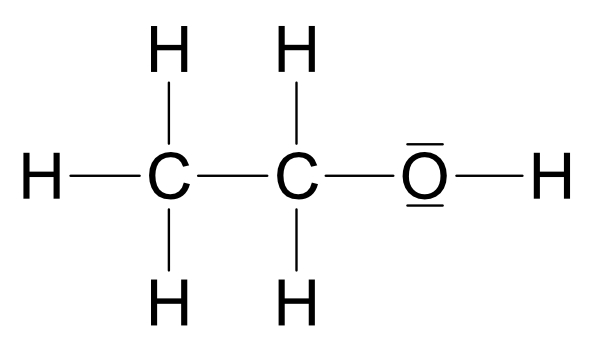
Ergebnis:
Ethanol (Struktur a) reagiert mit Natrium unter Wasserstoffbildung. Struktur b (Dimethylether) würde so nicht reagieren, da sich kein Proton abspalten kann. Somit besitzt Ethanol die Strukturformel:
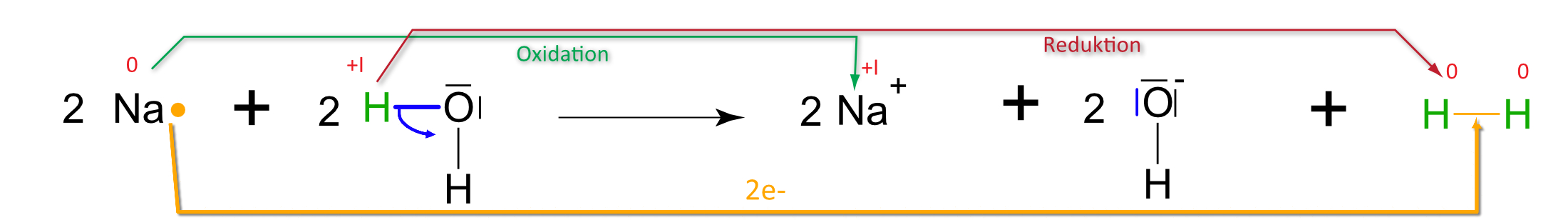
1. Natrium + Wassera) Teilchengleichung (mit Strukturformeln)
2 Na (s) + 2 H₂O (l) → 2 NaOH (aq) + H₂ (g) Natrium Wasser Natriumhydroxid Wasserstoff fest flüssig gelöst gasförmig 2. Natrium + Ethanol
Man kann Ethanol ja als Derivate (=Abkömmlinge) von Wasser betrachten. Wasser hat ein Sauerstoff-Atom und zwei Wasserstoff-Atome; Ethanol hat ein Sauerstoff-Atom, ein Wasserstoff-Atom und eine Ethyl-Gruppe. Beim Ethanol ist also ein Wasserstoff-Atom durch eine Ethylgruppe ersetzt. Wenn wir diese Alkylgruppe als "Rest" betrachten, dann zeigt sich die Verwandtschaft von Ethanol mit Wasser. Hat man also die Reaktionsgleichung von Wasser mit Natrium verstanden, dann müsste einem auch die Reaktionsgleichung von Ethanol (und anderen Alkoholen) leichtfallen. Versucht nun einmal, die Reaktion von Natrium mit Ethanol zu formulieren.
a) Teilchengleichung (mit Strukturformeln)
{slider title="Lösung" open="false" class="icon"}
{/sliders}
b) Reaktionsgleichung{slider title="Lösung" open="false" class="icon"}
2 Na (s) + 2 C₂H₅OH (l) 2 NaC₂H₅O (aq) + H₂ (g){/sliders}
Auswertung: Es ist keine „klassische“ Säure-Base-Reaktion nach Brönstedt. Grund: +I-Effekt (vgl. unten) der Methylgruppe (Protonierung ist erschwert). Es handelt sich hier um eine Redoxreaktion (Veränderung der Oxidationenszahlen). Formal geben zwei Moleküle Ethanol je ein Proton ab. Jedes Proton nimmt von einem Natrium- bzw. Lithiumatom ein Elektron auf; es bilden sich so zwei Wasserstoffatome, die sich zu einem Wasserstoffmolekül zusammenlagern. Analog, nur heftiger, verläuft die Reaktion mit Wasser.
Weitere Übungen:
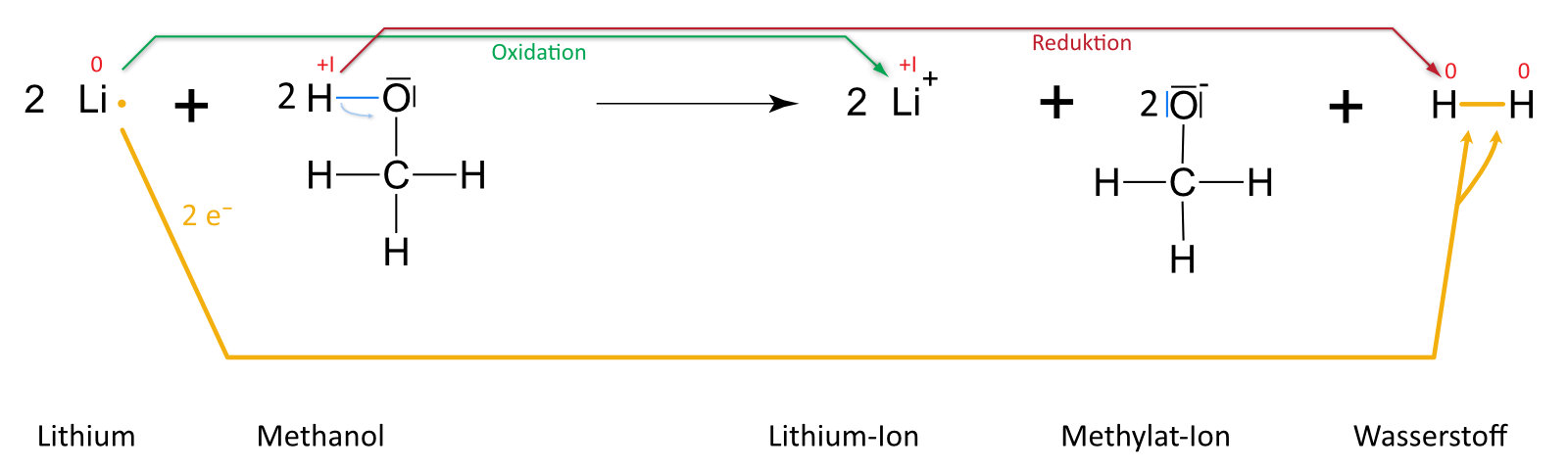
Lithium und Methanol
Formuliert auch dafür die Reaktionsgleichung (vgl. oben)
{slider title="Lösung" open="false" class="icon"}
{/sliders}
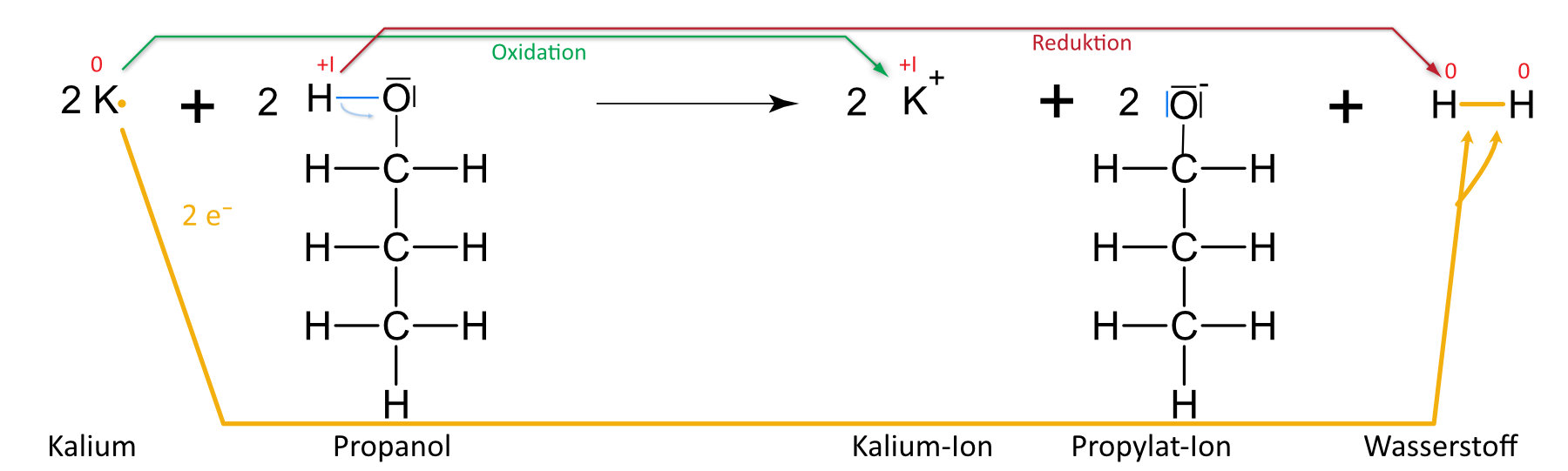
Kalium und Propanol
{slider title="Lösung" open="false" class="icon"}
{/sliders}