Was du in diesem Kapitel lernst
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung – der charakteristischen funktionellen Gruppe dieser Verbindungsklasse. Am Beispiel des Ethens (C2H4) lernst du Aufbau, Eigenschaften und typische Reaktionen der Alkene kennen: von der Bromwasserprobe über die cis-trans-Isomerie bis zur katalytischen Hydrierung.
Grundlagen aus der 10. Klasse
Alkene bauen direkt auf dem Wissen über die gesättigten Kohlenwasserstoffe auf – wiederhole bei Bedarf: → 1. Alkane – Homologe Reihe, Genfer Nomenklatur, radikalische Substitution
Kapitelübersicht – 2. Alkene
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkene sind ungesättigte Kohlenwasserstoffe. Ihre charakteristische funktionelle Gruppe ist die C=C-Doppelbindung (σ- + π-Bindung). Allgemeine Formel: CnH2n.
Nachweis
Die Bromwasserprobe weist C=C-Doppelbindungen nach: Braunes Bromwasser wird durch Additionsreaktion entfärbt – eindeutiger Nachweis auf Mehrfachbindungen.
cis-trans-Isomerie
Die Doppelbindung blockiert die freie Rotation um die C=C-Achse. Dadurch entstehen räumlich verschiedene cis- und trans-Isomere mit unterschiedlichen Eigenschaften.
Reaktionstyp
Typisch für Alkene ist die elektrophile Addition: Die Doppelbindung wird geöffnet, Atome oder Gruppen lagern sich an (z. B. H2, Br2, HBr).
Häufige Fragen – Alkene
Was sind Alkene und wie unterscheiden sie sich von Alkanen?
Alkene sind Kohlenwasserstoffe mit mindestens einer C=C-Doppelbindung. Im Gegensatz zu den gesättigten Alkanen (nur Einfachbindungen) sind Alkene ungesättigt: Die Doppelbindung besteht aus einer σ-Bindung und einer π-Bindung. Die allgemeine Summenformel lautet CnH2n. Das einfachste Alken ist Ethen (C2H4). Alkene sind durch ihre Doppelbindung reaktiver als Alkane; ihr typischer Reaktionstyp ist die elektrophile Addition, nicht die radikalische Substitution der Alkane.
Wie weist man eine C=C-Doppelbindung nach?
Den klassischen Nachweis liefert die Bromwasserprobe: Braunes Bromwasser (Br2 in Wasser) wird durch Additionsreaktion entfärbt, weil das Brom an die Doppelbindung addiert wird. Gleichung am Beispiel Ethen: C2H4 + Br2 → C2H4Br2 (1,2-Dibromethan). Der Test ist eindeutig für alle Verbindungen mit Mehrfachbindungen. → 2.1.5 Nachweis von Alkenen
Was ist cis-trans-Isomerie, und wann tritt sie auf?
Die C=C-Doppelbindung blockiert die freie Drehbarkeit um die Bindungsachse. Wenn an beiden Doppelbindungskohlenstoffen je zwei verschiedene Substituenten sitzen, entstehen zwei räumlich unterschiedliche Isomere: Im cis-Isomer (= Z-Form: zusammen) stehen die gleichartigen Gruppen auf derselben Seite der Doppelbindung; im trans-Isomer (= E-Form: entgegen) auf gegenüberliegenden Seiten. Beispiel: cis-But-2-en und trans-But-2-en haben dieselbe Summenformel (C4H8), aber verschiedene Siedepunkte. → 2.1.6/2.1.7 Isomerien von Alkenen
Wie werden Alkene nach IUPAC benannt?
Die Nomenklatur der Alkene folgt denselben Grundregeln wie bei den Alkanen, mit Besonderheiten: (1) Die längste Kette, die die Doppelbindung enthält, ist die Hauptkette. (2) Sie wird so nummeriert, dass die Doppelbindung die niedrigstmögliche Lokante erhält. (3) Die Endung lautet „-en" (mehrere Doppelbindungen: -dien, -trien). (4) Die Position der Doppelbindung steht als Lokant vor der Endung: z. B. But-1-en, nicht 1-Buten (moderne IUPAC-Schreibweise). Bei cis-trans-Isomeren wird das Konfigurationspräfix vorangestellt: cis-But-2-en oder (Z)-But-2-en. → 2.2 Nomenklatur der Alkene
Was ist katalytische Hydrierung, und wie verhält sie sich zur Eliminierung?
Katalytische Hydrierung und Eliminierung sind Umkehrreaktionen: Bei der Hydrierung wird H2 mithilfe eines Nickel- oder Platin-Katalysators an die C=C-Doppelbindung addiert → Alken wird zu Alkan (z. B. C2H4 + H2 → C2H6). Bei der Eliminierung wird H2 unter hoher Temperatur abgespalten → Alkan wird zu Alken. Die Gesamtreaktion ist umkehrbar: Ethen ⇔ Ethan. Wichtig: Der Katalysator beeinflusst nur die Reaktionsgeschwindigkeit, verschiebt aber die Gleichgewichtslage nicht. → 2.3 Katalytische Hydrierung
Lernkarten – Alkene
Klicke auf eine Karte, um die Antwort zu sehen.
Was ist die funktionelle Gruppe der Alkene, und woraus besteht sie?
Die C=C-Doppelbindung. Sie besteht aus einer σ-Bindung (Überlappung entlang der Achse) und einer π-Bindung (seitliche Überlappung). Alkene sind deshalb ungesättigt und reaktiver als Alkane.
Wie lautet die allgemeine Formel der Alkene? Nenne die ersten vier mit Formel.
CnH2n (n ≥ 2)
Ethen C2H4 · Propen C3H6
Buten C4H8 · Penten C5H10
Wie funktioniert der Bromwassertest? Was beobachtet man?
Braunes Bromwasser wird mit dem Alken gemischt. Das Bromwasser entfärbt sich, weil Br2 durch elektrophile Addition an die C=C-Doppelbindung gebunden wird. → Nachweis auf Mehrfachbindung.
Wann tritt cis-trans-Isomerie auf? Was unterscheidet cis von trans?
Wenn an beiden C-Atomen der C=C-Bindung je zwei verschiedene Substituenten sitzen. cis: gleichartige Gruppen auf einer Seite; trans: auf gegenüberliegenden Seiten. Freie Rotation um die Doppelbindung ist nicht möglich.
Berechne: Wie viel g H2 werden benötigt, um 28 g Ethen vollständig zu hydrieren?
C2H4 + H2 → C2H6
M(C2H4) = 28 g/mol → n = 1 mol
Stöchiometrie 1:1 → n(H2) = 1 mol
m(H2) = 1 mol · 2 g/mol = 2 g H2
Weiter im Fach Chemie / 10. Klasse
← 1. Alkane → 3. Alkine ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Aromaten – Benzol und seine Derivate · Cycloalkane
- Details
- Geschrieben von: Wolfram Hölzel
2 Alkene
2.1 Ethen
2.1.1 Eigenschaften
- farbloses, brennbares Gas;
- die Flamme leuchtet stärker als bei Methan und Ethan;
- Siedetemperatur: -104°C
- Schmelztemperatur: - 169°C
2.1.2 Ermittlung der Summenformel
a) Qualitative Analyse (Verbrennungsanalyse)
Bei der vollständigen Verbrennung von Ethen entstehen H2O und CO2.
b) Quantitative Analyse (Bestimmung der molaren Masse)
Die molare Masse von Ethen: M(Ethen) = 28 g/mol
Die Molekülmasse von Ethen: 28 u
c) Summenformel (Molekülformel): C2H4
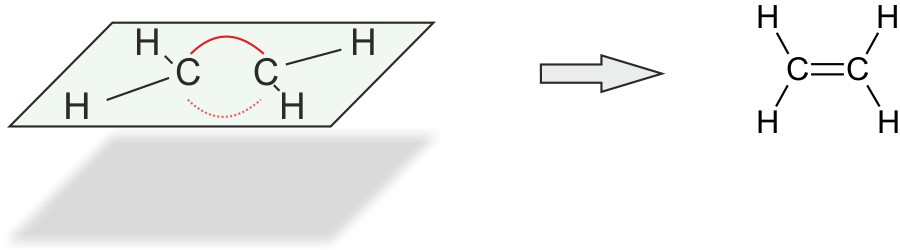
2.1.3 Strukturformel
Die Doppelbindung zwischen den beiden C-Atomen wird durch zwei Elektronenpaare gebildet. Diese stoßen sich ab. Man spricht von einer „Bogenbindung“ („Bananenbindung“).
Im Ethen Molekül betragen die Bindungswinkel 120°.
Alle Atome liegen in einer Ebene.
Die C=C-Doppelbindung verhindert die freie Drehbarkeit um die C-C-Achse.
Aufgabe: Wie viel Liter Luft benötigt man bei der Verbrennung von 2 l Ethen
{slider title="Lösung" open="false" class="icon"}
C2H4 + 3 O2 → 2 CO2 + 2 H2O
1 Molekül 3 Moleküle 2 Moleküle 2 Moleküle
Stoffmenge n: 1mol 3 mol 2 mol 2 mol
Mol. Volumen V 22,4 L 67,2 L 44,8 L
Dreisatz: x/2L = 67,7L/22,4L
Zur Vollständigen Verbrennung von 2 L Ethen benötigt man 6 L Sauerstoff, d.h. 30 L Luft.
{/sliders}
.
2.1.4 Vorkommen, Gewinnung und Verwendung
a) Vorkommen
Bei Pflanzen als Hormon (Phytohormon). Steuert:
- Fruchtreifung
- Keimwachstum
- Entwicklung
- Dickenwachstum
- Blattfall
- Informationsweitergabe an benachbarte Pflanzen
b) Gewinnung
- Cracken von Erdöl
c) Verwendung
- Reifung von Früchten
- Herstellung von organischen Stoffen (Kunststoffe, Tenside, ...)
- Details
- Geschrieben von: Wolfram Hölzel
2.1.5 Nachweis von Alkenen (Doppelbindung)
Versuch: Ein Erlenmeyerkolben wird unter Wasser mit 250 ml Ethen gefüllt, anschließend werden 0,5 ml Brom dazugegeben und mit dem Stopfen verschlossen.
Alternativ: Hexen + Bromwasser (VORSICHT FALLS MAN BROM NIMMT ⇨ heftige Reaktion)
Beobachtung:
Die Bromfarbe verschwindet; Volumenabnahme; der Erlenmeyerkolben wird warm; es entsteht ein flüssiges Produkt, die Dichte ist größer als 1 g/cm³.
Auswertung:
Zwei Hypothesen:
I) Substitution:
II) Addition:
Ergebnis
Bei der Reaktion Ethen + Brom entsteht (fast) nur ein Reaktionsprodukt. „Bromwasserstoffnebel“ waren kaum zu sehen. Es fand somit eine Addition statt.
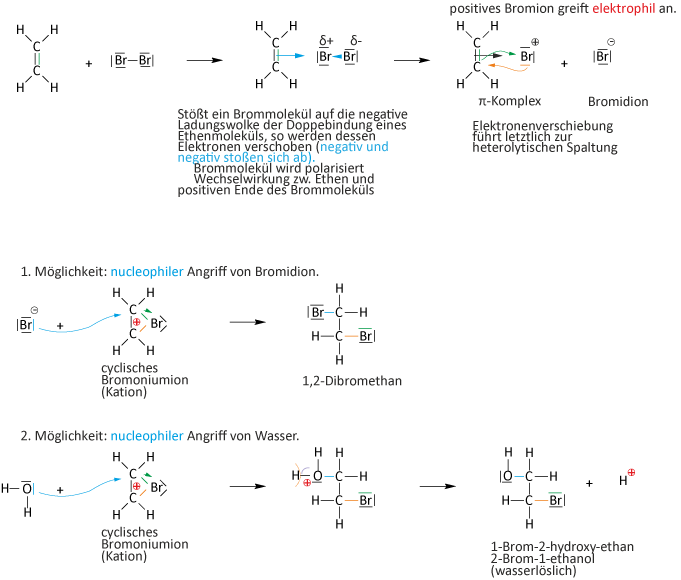
Additionsreaktionen: Reaktionen bei denen sich zwei Moleküle zu einem Molekül vereinigen! Es kommt dabei zur Anlagerung von Atomen oder Atomgruppen an Doppelbindungen (Mehrfachbindun-gen).
Reaktionsmechanismus: AE-Reaktionen (elektrophile Addition)
= typische Reaktion von Alkenen
- Details
- Geschrieben von: Wolfram Hölzel
2.1.6 Isomerien bei Ethenderivaten
Von Dichlorethen gibt es drei isomere Verbindungen:
2.1.7 cis-trans-Isomerie (bzw. E/Z-Isomerie
Die Doppelbindung blockiert die Drehbarkeit um die C-C-Bindungsachse. Die cis-trans-isomeren Verbindungen unterscheiden sich in ihrem physikalischen (und chemischen) Verhalten.
 |
 |
|
Dipol
|
kein Dipol (symmetrisch)
|
a) trans (lat) = hinüberschreiten, jenseits heute als (E)-Isomerie
Die wichtigen Substituenten (Alkylgruppen, Halogen-Atome, Hydroxylgruppe, ...) liegen auf der gegenüberliegenden Seite der Doppelbindung.
Heutzutage bezeichnet man es auch als (E)-Isomere, wobei (E) für entgegen gemerkt werden kann.
Beispiel: trans-But-2-en (= trans-2-Buten) = (E)-But-2-en.
c) cis (lat) = diesseits heute auch als (Z)-Isomere
Die wichtigen Substituenten liegen auf der gleichen Seite der Doppelbindung.
Heute auch als (Z)-Isomere von zusammen.
Beispiel: cis-But-2-en (=cis-2-Buten) = (Z)-But-2-en
Eselbrücke: cis: Ein cis-Molekül hat die Form wie ein "C" von "cis".
- Details
- Geschrieben von: Wolfram Hölzel
2.2 Nomenklatur der Alkene
Da die Nomenklatur der Alkene ähnlich zur Nomenklatur der Alkane ist, soll dieses Thema gleich als Übung besprochen werden. Schüler des Limes-Gymnasium Welzheims: siehe AB!
a) Nenne die homologe Reihe der Alkene bis Decen.
{slider title="Lösung - Homologe Reihe" open="false" class="icon"}
Hinweis: Methen kann es nicht geben; wie sollte bei einem C auch eine C=C-Doppelbindung entstehen. ;-)
Ethen - Propen - Buten - Penten - Hexen - Hepten - Octen - Nonen - Decen
{/sliders}
b) Zeichne die Strukturformeln von Propen, 1-Buten, cis-2-Buten, trans-2-Buten und 1,3-Butadien.
{slider title="Lösung" open="false" class="icon"}
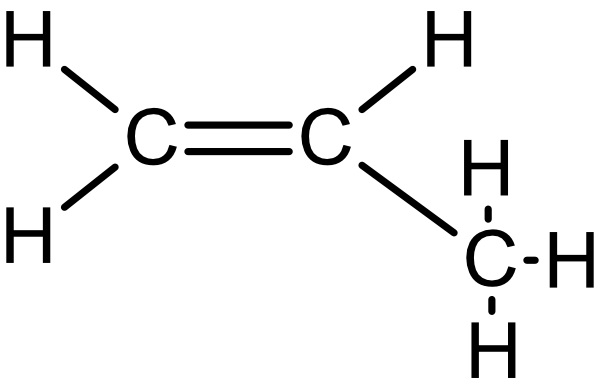
Propen:
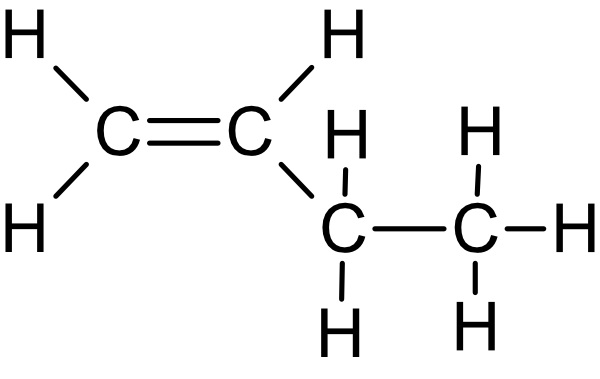
1-Buten:
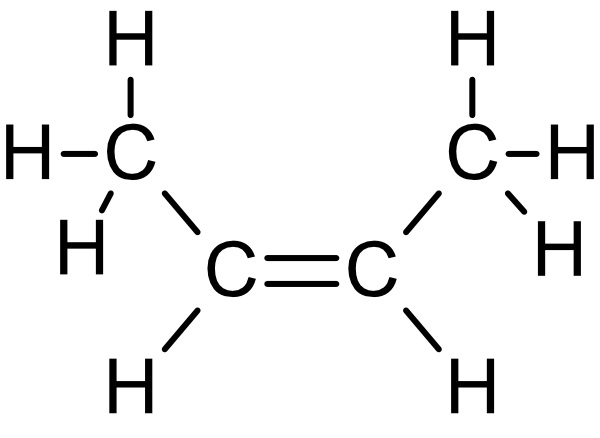
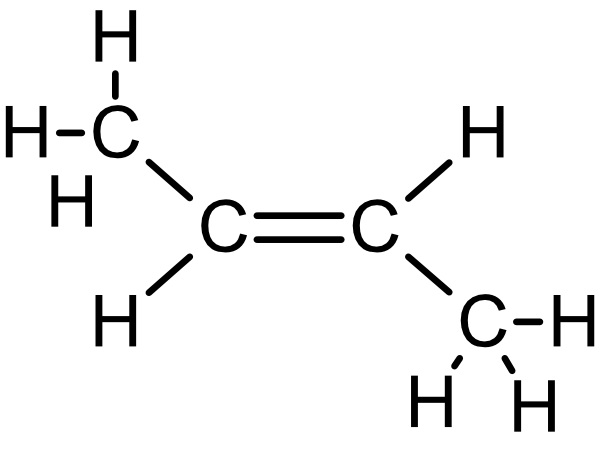
cis-2-Buten:
trans-2-Buten:
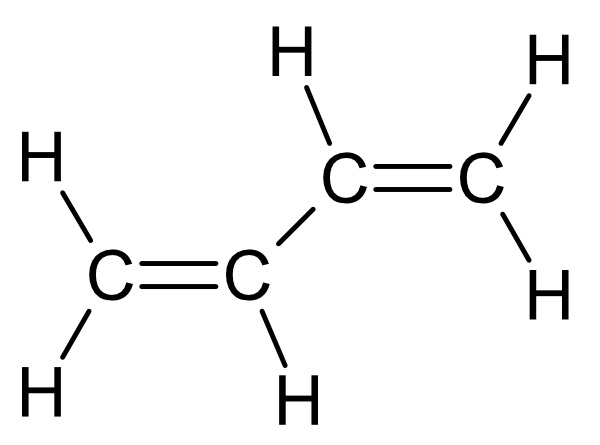
1,3 Butadien:
{/sliders}
c) Gib die Molekülformel von Propen an.
{slider title="Lösung - Molekülformel von Propen" open="false" class="icon"}
C₃H₆
{/sliders}
d) Benenne die folgende Verbindungen.
I:
II:
{slider title="Lösung" open="false" class="icon"}
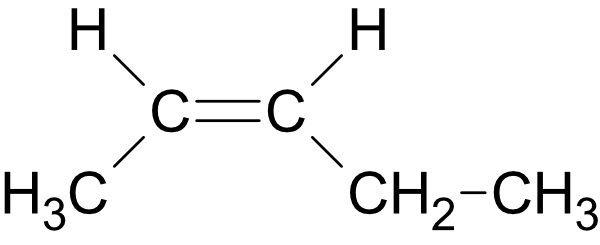
I.: Penta-1,3-dien
II. cis-Pent-2-en
{/sliders}
e) Zeichne die Strukturformeln der isomeren Pentene und benenne die Verbindungen.
{slider title="Lösung - Pentene" open="false" class="icon"}
Pent-1-en:
cis-Pent-2-en:
trans-Pent-2-en:
3-Methylbut-1-en:
2-Methylbut-2-en:
2.Methylbut-1-en:
{/sliders}
- Details
- Geschrieben von: Wolfram Hölzel